il sapone di marsiglia
Il sapone è un prodotto di massa destinato ad un pubblico vastissimo... tutti. Eppure, questo non è del tutto vero: c'è sapone e sapone! Si possono concepire prodotti di massa o prodotti di nicchia (destinati a particolari fruitori), ma ognuno di questi prodotti nasce puntando ad un target specifico.
Nel caso dei saponi, dato che "tutti" ne fanno uso, sembra ovvio che il target sia "tutti". Eppure, esistono saponi e detersivi, ognuno con un nome diverso, una confezione diversa, componenti diversi, un prezzo diverso. Il target generico è costituito dai "fruitori del detersivo e sapone", però un sottoinsieme di questo target è costituito da miriadi di "sotto-target", che danno ragione dell'esistenza di centinaia di prodotti diversi.
Uno di questi sotto-target è costituito da coloro che prediligono prodotti naturali, anallergici, delicati: i saponi (i detersivi sono prodotti di sintesi). All'interno di questo sotto-target, si possono individuare ulteriori sottoinsiemi che, comprendono le persone attente alla profumazione, quelle che desiderano che lo stesso prodotto possa essere usato per l'igiene personale, il bucato a mano e per quello in lavatrice; altri, al contrario diffidano di un unico prodotto adatto a tutte le esigenze. In breve, non è possibile accontentare tutti; tuttavia, il sapone di Marsiglia è certamente collocabile tra i prodotti il cui target è "coloro che prediligono prodotti naturali, anallergici, delicati".
La storia del sapone di Marsiglia è secolare e le regole di fabbricazione di questo diffusissimo e celebrato prodotto sono state fissate addirittura dal Re Sole, Luigi XIV. Tuttavia, l'attribuzione dell'origine di questo sapone alla città di Marsiglie non è corretta. Per darne ragione, occorre ricordare che a Gallipoli, un porto di rilevante importanza tra XVII e XIX secolo, si batteva il prezzo dell'olio per l'intera Europa. Qui nacque l'uso di addizionare la soda al sottoprodotto della lavorazione delle olive dal quale non si poteva ricavare più l'olio... ecco perché sarebbe più giusto chiamarlo sapone di "Gallipoli" e non sapone di Marsiglia.
 Il sapone vegetale di Marsiglia, è consigliato per detergere e rispettare lepidermide. Completamente vegetale e naturale al 100%, è ideale per la detersione di tutti i tipi di pelle, anche di quelle delicate, secche, disidratate e soggette ad arrossamenti.
Il sapone vegetale di Marsiglia, è consigliato per detergere e rispettare lepidermide. Completamente vegetale e naturale al 100%, è ideale per la detersione di tutti i tipi di pelle, anche di quelle delicate, secche, disidratate e soggette ad arrossamenti.
preparazione del sapone
La saponificazione consiste nella reazione d'idrolisi di un estere in ambiente basico e provoca la formazione di un alcool e del sale dell'acido corrispondente.
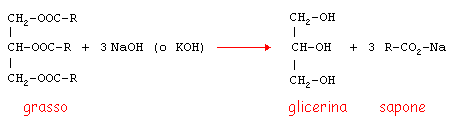
I saponi sono di solito sali di sodio di acidi carbossilici a lunga catena; vengono prodotti e usati per sciogliere le sostanze grasse nei processi di pulizia.
Il termine saponificazione è comunemente utilizzato in riferimento alla reazione di un idrossido di un metallo alcalino (base) con un grasso o un olio che dà origine al sapone.
Per preparare il sapone possiamo partire o da residui di grasso animale oppure, nel caso del sapone di gallipoli-marsiglia, partendo da olio di oliva (non è necessari che sia extra vergine, va bene anche quello di sansa e oliva) procedendo come segue:


- prelevare 12 ml di olio, 12 ml di una soluzione di NaOH al 20% (in commercio si trova a concentrazioni 30% e 48-50%) e mettere tutto in un recipiente da circa 250 ml;
- riscaldare a bagnomaria ad un temperatura di 60°/70° per circa mezz'ora, girando la miscela con una bacchetta di vetro;
- dopo circa 30 minuti aggiungere 10 ml di acqua (distillata) e mescolare per altri 60 minuti. La reazione di saponificazione è completa quando si osserva la comparsa di schiuma e la completa assenza di gocce di olio;
- aggiungere poi 60 ml di acqua bollente in modo da ottenere una pasta omogenea alla quale aggiungere 15 ml di una soluzione di NaCl (4 g NaCl ogni 10 ml);
- agitare molto bene per altri 5 minuti e lasciare decantare e raffreddare.
Il sapone formatosi, che si presenterà in scaglie, affiorerà separandosi dalla soluzione; poi verrà filtrato in un secondo recipiente ed in fine compattato in uno stampo in modo da conferirgli la forma di un panetto.

Prima della filtrazione sarebbe opportuno occorre controllare che non ci sia eccesso di NaOH: ciò si verifica con 3-4 gocce di fenolftaleina che in ambiente basico diventa rossa (in ambiente acido è incolore). In caso di basicità, si aggiunge qualche goccia di soluzione di HCl diluito.
Per ottenere un prodotto più delicato, più ricco di oli "liberi" e per sicurezza, si ricorre allo "sconto" della soda, riducendone la quantità usata del 5%. La pasta di sapone si può migliorare ulteriormente aggiungendo piccole quantità di crema emoliente, gocce di profumo e colorante.
 La soda caustica è una base fortissima e può provocare gravi ustioni. In soluzione al 20% non è particolarmente pericolosa, ma deve essere diluita con molta attenzione. VERSATE LA SODA LENTAMENTE NELL'ACQUA E MAI VICEVERSA: il liquido versato sulla soda provoca una reazione immediata con schizzi di materiale caustico molto pericolosi; la soda va versata in acqua lentamente, mentre si mescola. Per precauzione, effettuate la diluizione nel lavello. Non usare recipienti in alluminio: la soda reagisce con esso conferendo al sapone proprietà indesiderate.
La soda caustica è una base fortissima e può provocare gravi ustioni. In soluzione al 20% non è particolarmente pericolosa, ma deve essere diluita con molta attenzione. VERSATE LA SODA LENTAMENTE NELL'ACQUA E MAI VICEVERSA: il liquido versato sulla soda provoca una reazione immediata con schizzi di materiale caustico molto pericolosi; la soda va versata in acqua lentamente, mentre si mescola. Per precauzione, effettuate la diluizione nel lavello. Non usare recipienti in alluminio: la soda reagisce con esso conferendo al sapone proprietà indesiderate.
L'azione detergente del sapone è determinata dalla struttura molecolare dello stesso in cui esiste una parte lipofila apolare ( coda ) ed una parte idrofila polare ( testa ). Lo sporco grasso viene aggredito dalle code lipofile e ridotto in particelle ove le stesse code affondano; le particelle sono disperse nell'acqua per mezzo delle teste idrofili. L'azione meccanica porta al completo distacco dello sporco.
Le proprietà detergenti dipendono dalla capacità del sapone di formare emulsioni in cui le molecole del sapone stesso inglobano le particelle di sporco in un involucro solubile in acqua che ne permette la dispersione. Affinché il sapone possa esercitare con efficacia la sua azione detergente è necessaria un'acqua dolce (con contenuto basso di ioni Ca++ e Mg++), altrimenti si formano sali insolubili che allontanano dall'ambiente acquoso le molecole di sapone.
etichetta
Per distinguere i saponi dai detergenti è essenziale leggere le etichette. In entrambi i casi, i componenti sono elencati in sequenza dalla maggiore alla minore presenza (come per gli alimenti). Nel caso dei saponi, i grassi saponificati dovrebbero essere prevalenti ed essere citati in etichetta facendo precedere il termine sodium più quello del grasso anglo-latinizzato (es. sodium cocoate, sodium palmate, sodium palm kernelate, sodium olivate etc). Lo stesso discorso vale per il potassio (potassium palmate etc).
Gli ingredienti non saponificati, invece, devono essere indicati con il loro nome latino (botanico se si tratta di materiale vegetale, chimico se di composti). Si tratta di ingredienti di pregio che vengono aggiunti una volta completata la reazione di saponificazione (olii essenziali, succo daloe, olii emollienti, petali di fiori, semi, vitamine ecc.).

pianta di Jojoba |
Tutto ciò che non è sapone è detergente (o detersivo) e finisce comunque in ate (ad esempio ammonium lauryl sulfate, disodium laureth sulfosuccinate, ecc.). Si trovano inoltre innumerevoli altri ingredienti che possono essere conservanti, profumi, riempitivi (come la glicerina) e, nel caso in particolare degli shampoo, sequestranti. Questi ultimi sono sostanze che non permettono al calcare presente nellacqua di depositarsi sui capelli in modo che restino morbidi e si asciughino con facilità.
In fondo all'elenco sono indicati gli eventuali ingredienti di pregio, ad esempio il jojoba, nel caso degli shampoo all'olio di semi jojoba (Lo jojoba è l'unica tra le piante, grazie ai suoi semi, a contenere una cera liquida), è facile che sia fra gli ultimi ingredienti in elenco mentre il primo è sempre l'acqua (a meno che non si tratti di detergenti solidi come i saponi neutri).
Ultimi arrivati in commercio sono gli oli lavanti: si tratta di olii con aggiunta di emulsionanti che vengono utilizzati in genere per il lavaggio dei capelli. Al contatto con l'acqua, l'olio si emulsiona e con la sua presenza aiuta a rispettare la protezione grassa dei capelli.
 1 1 |
 2 2 |
 3 3 |
 4 4 |
 5 5 |
 6 6 |
 7 7 |
 8 8 |
 9 9 |
 10 10 |
 11 11 |
 12 12 |
13 |
 14 14 |
 15 15 |
 16 16 |
 HOME PAGE HOME PAGE |
Marcello Guidotti, copyright 2006
questa pagina può essere riprodotta su qualsiasi supporto o rivista purché sia citata la fonte e l'indirizzo di questo sito (ai sensi degli artt. 2575 e 2576 cc. Legislazione sul diritto d'autore). Le fotografie sono tratte da siti web e sono, o possono ritenersi, di pubblico dominio purché utilizzate senza fini di lucro. Le immagini di prodotti presenti nel sito hanno unicamente valenza esemplificativa oltre che, eventualmente, illustrare messaggi fuorvianti e non vi è alcun richiamo diretto o indiretto alla loro qualità e/o efficacia il cui controllo è affidato alle autorità regolamentatorie.
 Il sapone vegetale di Marsiglia, è consigliato per detergere e rispettare lepidermide. Completamente vegetale e naturale al 100%, è ideale per la detersione di tutti i tipi di pelle, anche di quelle delicate, secche, disidratate e soggette ad arrossamenti.
Il sapone vegetale di Marsiglia, è consigliato per detergere e rispettare lepidermide. Completamente vegetale e naturale al 100%, è ideale per la detersione di tutti i tipi di pelle, anche di quelle delicate, secche, disidratate e soggette ad arrossamenti.




