radiofarmaci e mezzi di contrasto
Al contrario delle immagini radiologiche (v. mezzi di contrasto), che vengono ottenute sfruttando l'attenuazione del fascio di raggi X da parte dei tessuti interposti tra l'apparecchiatura che le ha prodotte e il sistema di rilevazione, le immagini medico-nucleari vengono ottenute per mezzo della rilevazione di radiazioni emesse da radiofarmaci distribuiti nell'organismo. In un certo senso è il paziente che "emette" le radiazioni (gamma o X) che vengono registrate da apposite apparecchiature in grado di ricreare l'immagine corrispondente. Il nome "scintigrafie" dato alle immagini radiologiche, deriva dal termine "scintillazione": il fenomeno fisico sfruttato da queste apparecchiature per trasformare in energia elettrica l'energia quantica dei fotoni gamma o X.
Con il termine "radiofarmaci" si definiscono i preparati "radioattivi" con caratteristiche chimico-fisico-biologiche che rispettano tutte le normative previste dalla F.U. per la somministrazione nell'uomo. Il loro impiego diagnostico o terapeutico deve quindi essere preventivamente autorizzato, per ogni indicazione e modalità di somministrazione, dalle Autorità Sanitarie, come qualunque altro medicinale.
| radioisotopo |
impiego |
| Tecnezio 99 |
In vivo. Viene usato per scintigrafie sceheltriche, epatiche, renali, cerebrali, tiroidi per i bambini, funzionalità epatica. Tempo di dimezzamento: 6 ore |
| Iodio 131 |
In vivo. Usato per la tiroide, le renografie e il totalbody. Tempo di dimezzamento: 8 giorni. |
| Tallio 201 |
In vivo. Serve per scintigrafie del miocardio. Tempo di dimezzamento: 3 giorni. |
| Iodio 125 |
In vitro. Serve per tutte le analisi di radioimmunologia. Tempo di dimezzamento: 60 giorni. |
| Trizio |
Usato raramente. Tempo di dimezzamento: 12 anni circa. |
| Carbonio 14 |
Usato raramente. |
Il Dpr 185 del 1964 , unitamente ad una serie di decreti derivati, fornisce le indicazioni generali che regolano la detenzione, l'impiego e lo smaltimento del materiale radioattivo.
Storicamente, il primo radiofarmaco introdotto nella pratica clinica è stato lo 131I (Iodio-131), utilizzato nello studio delle patologie tiroidee. Sono stati poi progressivamente sviluppati altri radiofarmaci che, come lo 131I, avevano però caratteristiche fisiche e radio-biologiche non ottimali. Questo obbligava ad impiegarne quantitativi molto ridotti, che permettevano di ottenere solo immagini di qualità scadente, o precludevano del tutto la possibilità di ottenerle.
L'impulso decisivo alla crescita della medicina nucleare, che ne ha permesso la trasformazione da branca della radiologia a disciplina autonoma, è venuto dalla ideazione del primo generatore di 99mTc (Tecnezio 99 metastabile), costruito al Brookhaven Lab di New York nel 1958 e introdotto nell'uso clinico nel 1963.
 Fra tutti i radionuclidi proposti, il 99mTc ha dimostrato notevole utilità, in quanto i vecchi radionuclidi, oltre alle radiazioni gamma necessarie per ottenere le immagini, emettevano anche radiazioni beta che non servono ai fini diagnostici e sono molto più radiotossiche per i tessuti. Poi, il fatto che il 99mTc sia un metallo di transizione non presente in natura, e quindi non entra facilmente a far parte della struttura delle molecole biologiche, si è dimostrato un vantaggio: è diventato compito dei radio-chimici e radio-farmacisti identificare differenti sostanze che, legate al tecnezio, fossero in grado di concentrarsi in organi diversi.
Fra tutti i radionuclidi proposti, il 99mTc ha dimostrato notevole utilità, in quanto i vecchi radionuclidi, oltre alle radiazioni gamma necessarie per ottenere le immagini, emettevano anche radiazioni beta che non servono ai fini diagnostici e sono molto più radiotossiche per i tessuti. Poi, il fatto che il 99mTc sia un metallo di transizione non presente in natura, e quindi non entra facilmente a far parte della struttura delle molecole biologiche, si è dimostrato un vantaggio: è diventato compito dei radio-chimici e radio-farmacisti identificare differenti sostanze che, legate al tecnezio, fossero in grado di concentrarsi in organi diversi.
Grazie alle conoscenze acquisite sulle sue proprietà chimiche, oggi il 99mTc è il radionuclide ideale e quindi il più utilizzato nella pratica clinica: rappresenta oltre il 90% dei radionuclidi impiegati in diagnostica. La sua ampia diffusione è anche legata al fatto che prima che esso fosse disponibile, tutti i radionuclidi utilizzati venivano prodotti solo in alcuni grandi centri nucleari, prevalentemente negli Stati Uniti e in Canada, da cui venivano spediti per via aerea ai singoli laboratori che li richiedevano caso per caso. E' facile immaginare il costo di questa procedura. Il 99mTc ha un'emivita (6 h) sufficientemente lunga per gli esami diagnostici e tale da permettere la dimissione del paziente in breve tempo.
Il Tecnezio può essere definito, in modo un pò provocatorio, un ECO-nuclide, nel senso che è "ECOlogico" perché emette solo radiazioni gamma, di energia adatta per ottenere immagini, e non contamina l'ambiente avendo una semivita (il tempo in cui dimezza spontaneamente la sua radioattività) di sole 6 ore; il che vuol dire che qualunque quantitativo di radioattività dovesse - ad esempio - entrare nel sistema fognario tramite le urine o le feci dei pazienti, si auto-esaurirebbe in un paio di giorni (è vero solo per modesti quantitativi, decine di grammi. NdR). "ECOnomico" perchè il generatore che lo produce fornisce gran parte della radioattività necessaria al funzionamento di un Centro di medicina nucleare di medie dimensioni, per un'intera settimana, ad un costo di 1000-1500 euro.
il generatore di radionuclidi 99Mo  99 mTc 1
99 mTc 1
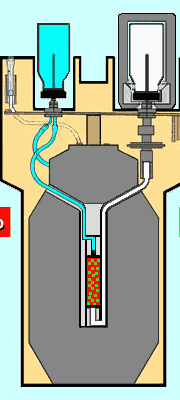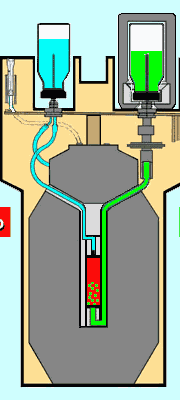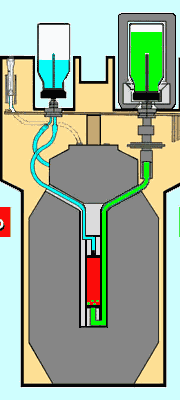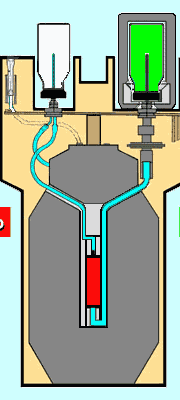
In figura è mostrato lo schema della sezione di un tipico generatore di 99mTc, le cui dimensioni reali sono circa 30 x 15 x 15 cm.
Il meccanismo di funzionamento è relativamente semplice:
Il Molibdeno (numero atomico 32) e il Tecnezio (numero atomico 43) sono due elementi chimicamente differenti; è quindi possibile scegliere una resina "a scambio ionico" con caratteristiche tali da legare in modo indissolubile il Molibdeno, lasciando invece completamente libero il Tecnezio. Una colonnina sterile di tale resina è il "cuore" del generatore
99Mo  99 mTc
99 mTc
questa, dopo che è stato adsorbito il 99Mo, viene introdotta in un contenitore di piombo (in grigio, al centro del disegno) di spessore adeguato (alcuni cm) per frenare le radiazioni gamma emesse dal 99Mo, che sono di energia elevata (fino a 1 MeV). Il 99Mo decade, con una emivita di 66 ore, a 99 mTc che a sua volta decade a 99Tc (cessando di essere radioattivo) con un'emivita di 6 ore. Sulla colonnina, in mancanza di interventi esterni, sono quindi presenti, in equilibrio fra loro, sia il 99Mo (in rosso nel disegno) sia il 99mTc (in verde nel disegno).
Alle due estremità della colonnina sono collegati due tubicini che finiscono in altrettanti aghi fissati in due alloggiamenti (per accogliere i flaconcini di eluizione e di raccolta) posti sulla parte superiore del generatore. Per eluire il 99mTc si infila, in uno dei due aghi, un flaconcino in vetro - con tappo in gomma perforabile - contenente soluzione fisiologica sterile (in celeste nel disegno); nel secondo ago si infila un altro flaconcino, simile al primo, ma "vuoto d'aria" (in bianco nel disegno) e inserito in un contenitore schermato (piombo o tungsteno). La depressione creata dal vuoto provoca lo svuotamento del flaconcino contenente la soluzione fisiologica che "lava" la colonnina di resina, asportandone il solo 99 mTc che, al termine dell'eluizione, è tutto contenuto nel secondo flaconcino, pronto per essere utilizzato per marcare i vari radiofarmaci (il 99Mo rimane intrappolato nella resina).
Subito dopo l'eluizione, la colonnina contiene quindi solo 99Mo; tuttavia, il suo decadimento continua e così inizia subito a formarsi nuovo 99 mTc. Il processo di rigenerazione procede con andamento esponenziale e, in una emivita (6 ore) si rigenera il 50% del 99 mTc, dopo 12 ore il 75% e dopo 18 ore il 90% circa. Dopo 4 emivite (24 ore) il 99 mTc è praticamente ricostituito e il generatore è pronto per essere nuovamente eluito. Ovviamente, poichè nel frattempo il 99Mo è decaduto, non si otterrà più la stessa quantità di 99mTc del giorno prima, bensì circa il 70%.
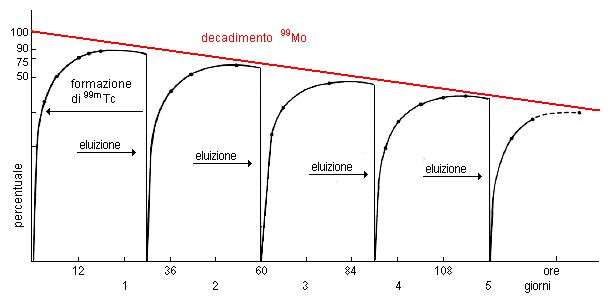 |
| Il grafico mostra la generazione (percentuale) di 99 mTc mentre il 99 Mo decade. Si noti come le eluizioni effettuate ogni 24 ore abbiano una resa sempre minore.
|
requisiti dei radiofarmaci
I radioisotopi che emettono prevalentemente radiazioni alfa e beta, sono assorbiti quasi totalmente da strutture biologiche di piccolo spessore (pochi micron o pochi millimetri al massimo) e questo non li rende adatti per applicazioni medico-nucleari diagnostiche, che sono basate sulla rilevazione esterna della distribuzione di radiofarmaci all'interno dell'organismo vivente. Così, per scopi diagnostici in vivo sono impiegati radioisotopi che emettono prevalentemente radiazioni gamma di energia idonea per la loro misura mediante gli strumenti medico-nucleari più comunemente utilizzati, cioè le gamme camere.
I radiofarmaci vengono somministrati direttamente al paziente, per via orale o endovenosa. Le somministrazioni non causano danni (comunque irrilevanti rispetto al vantaggio derivante da una diagnosi precoce) in quanto le dosi impiegate sono minime e i radioisotopi impiegati hanno tossicità ed energia molto bassa. Inoltre i nuclidi hanno tempi di vita media piuttosto ridotti e nel radiofarmaco sono generalmente presenti quantità di atomi inattivi che diminuiscono l'attività specifica del prodotto (radioattività per unità di massa dell'elemento, generalmente espressa in MBq o GBq / grammo).
Per comprendere i requisiti legati all'efficacia di un radiofarmaco, a titolo di esempio, possiamo individuare quelli richiesti (soddisfatti dal 99mTc) per permettere una misura accurata del flusso plasmatico renale efficace (FPRE):
- essere eliminato esclusivamente dai reni;
- essere totalmente eliminato dal sangue arterioso durante il transito attraverso il rene;
- non venire metabolizzato;
- volume di distribuzione uguale al volume plasmatico. Il legame con le proteine plasmatiche è irrilevante se la dissociazione è rapida e non influisce sulla frazione di estrazione; un legame con le proteine plasmatiche può, anzi, essere utile perché può ridurre il volume di distribuzione.
radiofarmaci per terapia
L'uso della medicina nucleare in terapia si fonda sul fatto che il radiofarmaco somministrato al paziente, concentrandosi nei tessuti patologici (perché affine, o per scarsa diffusività), possa irradiarli e distruggerli risparmiando, per quanto possibile, quelli sani. I radiofarmaci che vengono usati in terapia sono, per lo più differenti rispetto a quelli usati in diagnostica in quanto emettono radiazioni corpuscolate in grado di dissipare tutta la loro energia in uno spazio molto piccolo (<1 cm); ciò permette una radioterapia metabolica selettiva e mirata. Ovviamente, come avviene per gli usi diagnostici anche per gli usi terapeutici è fondamentale una costante ricerca per la messa a punto di nuovi radiofarmaci che presentino sempre migliori caratteristiche fisiche e farmacologiche.
Un esempio di beta emettitore è quello del Re-186/188, emettitore beta-gamma: se legato a specifici anticorpi o altre sostanze ad attività recettoriale, esso può consentire sia il trattamento in loco di masse tumorali che studi di biodistribuzione.
Le particelle alfa sono di notevole interesse per le applicazioni in terapia in quanto il loro ridotto raggio d'azione nei tessuti molli è limitato al diametro di poche cellule. Il rilascio di un'elevata energia in un piccolo volume, rende le particelle alfa particolarmente adatte per il targeting di micrometastasi e di cellule tumorali singole come la leucemia e altre malattie ematiche. Particolarmente interessante per le sue proprietà nucleari uniche, è il radioisotopo bismuto-213, caratterizzato da un'emivita di 45 minuti e un'emissione di particelle alfa ad alta energia (8,4 MeV). La sua disponibilità dal sistema generatore attinio-225/bismuto-213 rende questo radioisotopo particolarmente adatto per uso medico. L'attinio-225 è formato dal decadimento radioattivo del radio-225, il prodotto di decadimento del torio-229, a sua volta ottenuto dal decadimento dell'uranio-233.
Il brevissimo tempo di dimezzamento del bismuto-213, pone dei limiti di bismuto suo utilizzo, reso possibile solo quando la sua combinazione con una molecola vettore può essere condotta molto rapidamente e il targeting è ottenuto rapidamente, come il trattamento clinico della leucemia mieloide acuta per via endovenosa.
1
Il testo e le immagini (salvo l'animazione ricostruita come GIF animata, la tabella in testa ed alcune modifiche necessarie per chiarezza) sono tratte da: http://www.unipd.it/nucmed/TF/TF.pharm.ita.html
mezzi di contrasto in radiologia tradizionale
I radiofarmaci non devono essere confusi con i mezzi di contrasto: mentre i primi fanno temporaneamente diventare il corpo una sorgente di radiazione da rilevare con apposita strumentazione, i mezzi di contrasto permettono alle radiazione (emesse da una sorgente esterna) di essere assorbite da quelle parti del corpo che diversamente non sarebbero rilevabili. Vediamone la ragione.
In una immagine (fotografia, filmato, disegno), il contrasto è determinato dalla diversa riflessione della luce sulle varie zone che la compongono: se la differenza di luminosità fra le zone è bassa si ha scarso contrasto e le zone si confondono le une con le altre (per es. un bicchiere di vetro trasparente su uno sfondo bianco); se la differenza di luminosità fra le zone è alta, queste si distinguono più facilmente le une dalle altre (per es. un bicchiere di vetro colorato su uno sfondo bianco). Nel caso di una immagine diagnostica, il contrasto delle immagini dipende dalle diverse densità, dagli spessori delle strutture attraversate (contrasto naturale) e dalla costituzione anatomica degli organi attraversati (il loro numero atomico Z).
In generale, per poter radiografare una parte od un organo del corpo umano, è necessario che la parte che si vuole osservare abbia un coefficiente di assorbimento nettamente diverso rispetto alle parti circostanti. Poiche´ il coefficiente di assorbimento cresce molto rapidamente al crescere del numero atomico della sostanza, si comprende perché le ossa siano visibili ai raggi X. Le ossa, costituite sostanzialmente da calcio (numero atomico medio Z = 13.8), sono circa 40 volte più opache dei tessuti circostanti, formati in gran parte da acqua (numero atomico medio di circa Z = 6.5) e quindi poco o nulla visibili. Questo significa che se viene eseguita una radiografia diretta (cioè senza mezzo di contrasto) dell'addome, tutti gli organi che vi sono contenuti non sono visibili, perché hanno una densità uniforme, quindi l'immagine che ne risulta è uniformemente grigia. Così, per radiografare un organo, è necessario creare artificialmente un contrasto tra lo stesso stomaco e le strutture che lo circondano. Per esempio, nel caso dello stomaco, è necessario riempirlo con una sostanza opaca ai raggi X, come ad esempio il Bario (in forma di sale, BaSO4), che possiede un elevato numero atomico (Z = 56). Dunque, in radiologia è possibile anche ottenere un contrasto artificiale; queste indagini prendono perciò il nome di esami radiologici con mezzo di contrasto.
I mezzi di contrasto sono suddivisi in radiopachi e radiotrasparenti.
- radiopachi: sono rappresentati da elementi ad alto numero atomico (Z) e comprendono il solfato di bario ed i composti dello iodio (iodati). Questi ultimi, sono a loro volta suddivisi in inorganici ed organici. Gli inorganici sono rappresentati da preparati oleosi il cui impiego è attualmente limitato allo studio del sistema linfatico. Gli organici sono rappresentati da preparati idrosolubili e precisamente da molecole organiche che veicolano tre o più atomi di iodio. Essi si eliminano attraverso il rene od il fegato.
- radiotrasparenti: contengono elementi a basso numero atomico quali l'ossigeno, il carbonio, l'azoto. Essi sono rappresentati dall'aria filtrata, dall'anidride carbonica e dal protossido di azoto.
Un efficace mezzo di contrasto deve possedere le seguenti caratteristiche generali:
- elevata radio opacità (elevato numero atomico);
- buona tollerabilità: la tossicità deve essere molto bassa;
- assenza di attività farmacologica: la funzionalità di organi ed apparati non deve essere modificata;
- rapida e totale eliminazione da parte dell’organismo;
- si richiede un particolare tropismo per determinati organi (rene, fegato).
Dal punto di vista pratico è conveniente dividere i mezzi di contrasto in quattro categorie principali:
- mezzi di contrasto per il tubo digerente: il solfato di bario è un sale pochissimo solubile e opaco ai raggi X. Queste caratteristiche sono molto utili nella pratica medica per la diagnosi di occlusioni gastro intestinali attraverso l'ingestione del sale stesso e successiva radiografia dell'addome (sebbene il solfato di bario sia altamente tossico, la sua scarsissima solubilità lo rende di fatto innocuo e viene eliminato senza problemi per il paziente).
Oltre al solfato di bario, sono disponibili per lo studio del tubo digerente anche mezzi di contrasto idrosolubili, che vengono utilizzati selettivamente nel caso di sospetta perforazione in quanto, a differenza del bario, se penetrano nel peritoneo non creano problemi.
- mezzi di contrasto ad eliminazione biliare: si tratta di composti iodati che, introdotti per via orale od iniettati in una vena, vengono assorbiti dall'intestino, giungono al fegato e da esso vengono eliminati attraverso la bile, che risulta opaca nell'immagine radiologica.
- mezzi di contrasto ad eliminazione renale: oggi sono utilizzati quelli definiti - con evidente messaggio d'innovazione - di "terza generazione" e sono composti idrofilici caratterizzati da ridottissima tossicità. Essi percorrono il torrente circolatorio e vengono eliminati dal rene. Nel caso di funzionalità renale ridotta, altri organi possono assumere una funzione cooperativa nell'eliminazione di questo tipo di contrasto (fegato, intestino tenue, ghiandole salivari).
I mezzi di contrasto ad eliminazione renale sono quelli più largamente impegnati in quanto, oltre allo studio dell'apparato urinario, consentono lo studio dei vasi arteriosi e venosi; sono quindi alla base rispettivamente delle tecniche arteriografiche e flebografiche. Essi sono inoltre impiegati in varie applicazioni nella TC (tomografia computerizzata) dell'encefalo, del torace, dell'addome e della pelvi, nella radiografia del midollo spinale (mieloradiografia), delle articolazioni (artrografia) ed in quella dell'utero e delle tube (isterosalpingografia).
- mezzi di contrasto per linfografia: il mezzo di contrasto attualmente più utilizzato è il Lipiodol®, che risulta formato da una mescolanza di acidi grassi quali quello oleico, linoleico, palmitico e stearico, legati allo iodio. Dopo essere stato iniettato in un vaso linfatico periferico del dorso del piede, inizialmente riempie i vasi linfatici di tutto il corpo e poi i linfonodi. Lascia poi presto i vasi linfatici rimanendo viceversa presente nei linfonodi per settimane e mesi. Il mezzo di contrasto che non rimane nei linfonodi passa nel sistema venoso e raggiunge i piccoli vasi polmonari, dove viene intrappolato per poi essere rimosso dai macrofagi. L'impiego della linfografia è rivolto soprattutto alla ricerca ed allo studio di tumori originati nei linfonodi e di alcuni tumori che hanno invece dato metastasi nei linfonodi.
mezzi di contrasto utilizzati in tomografia computerizzata (TAC): sono impiegati sia mediante somministrazione orale che endovena (iv). I primi sono simili a quelli iodati idrosolubili che sono utilizzati per l'esame radiologico dell'apparato digerente. L'impiego di questi mezzi di contrasto è riservato agli esami TAC dell'addome ed ha lo scopo di mettere in evidenza le anse intestinali rispetto alle circostanti strutture di altri organi e vasi. I mezzi di contrasto iv sono rappresentati da quelli di tipo non ionico che vengono eliminati con le urine tramite il rene. Il loro impiego trova ragione nella migliore evidenziazione delle lesioni, nella caratterizzazione della natura delle stesse e nella valutazione dell'estensione di una malattia.
mezzi di contrasto utilizzati in risonanza magnetica (RMN): sono rappresentati dai composti a base di una sostanza chiamata Gadolinio (Gd). Tali mezzi di contrasto esplicano la loro azione in modo completamente diverso da quelli iodati impiegati in radiologia. Infatti essi esaltano il contrasto tra i tessuti perché dotati di proprietà magnetiche; per questo sono chiamati paramagnetici. Dopo essere stati somministrati per via endovenosa, si distribuiscono prima nei vasi sanguigni e poi anche negli spazi extra-vascolari; successivamente vengono eliminati dai reni e, in misura minore, attraverso l'intestino. Le principali indicazioni all'impiego dei mezzi di contrasto paramagnetici riguardano le malattie del sistema nervoso centrale (encefalo e midollo spinale), lo scheletro (tumori ed infezioni), cuore, fegato e reni.
produzione di radiofarmaci
Tutti radionuclidi sfruttati in terapia vengono prodotti artificialmente per mezzo di: ciclotroni; generatori di radionuclidi (es. quello del tecnezio); reattori nucleari.
 |
| produzione di radiofarmaci. Da sinistra: ciclorone; generatore di nuclidi; reattore nucleare (le illustrazioni non sono in scala) |
riferimenti normativi
Decreto Legislativo 24 aprile 2006, n. 219
Farmacopea Ufficiale della Repubblica Italiana XII Ed.
Norme di Buona Preparazione dei radiofarmaci per medicina nucleare 30.3.2005
Art. 7.
Radiofarmaci preparati al momento dell'uso
L 'AIC non è richiesta per i radiofarmaci preparati al momento dell'uso, secondo le istruzioni del produttore, da persone o stabilimenti autorizzati ad usare tali medicinali, in uno dei centri di cura autorizzati e purché il radiofarmaco sia preparato a partire da generatori, kit o radiofarmaci precursori per i quali sia stata rilasciata l'AIC. |
 1 1 |
 2 2 |
 3 3 |
 4 4 |
 5 5 |
 6 6 |
 7 7 |
 8 8 |
 9 9 |
 10 10 |
 HOME PAGE HOME PAGE |
Marcello Guidotti, copyright 2010-2011-2013
 Fra tutti i radionuclidi proposti, il 99mTc ha dimostrato notevole utilità, in quanto i vecchi radionuclidi, oltre alle radiazioni gamma necessarie per ottenere le immagini, emettevano anche radiazioni beta che non servono ai fini diagnostici e sono molto più radiotossiche per i tessuti. Poi, il fatto che il 99mTc sia un metallo di transizione non presente in natura, e quindi non entra facilmente a far parte della struttura delle molecole biologiche, si è dimostrato un vantaggio: è diventato compito dei radio-chimici e radio-farmacisti identificare differenti sostanze che, legate al tecnezio, fossero in grado di concentrarsi in organi diversi.
Fra tutti i radionuclidi proposti, il 99mTc ha dimostrato notevole utilità, in quanto i vecchi radionuclidi, oltre alle radiazioni gamma necessarie per ottenere le immagini, emettevano anche radiazioni beta che non servono ai fini diagnostici e sono molto più radiotossiche per i tessuti. Poi, il fatto che il 99mTc sia un metallo di transizione non presente in natura, e quindi non entra facilmente a far parte della struttura delle molecole biologiche, si è dimostrato un vantaggio: è diventato compito dei radio-chimici e radio-farmacisti identificare differenti sostanze che, legate al tecnezio, fossero in grado di concentrarsi in organi diversi.