pubblicità del sistema ClindesseTM
Sulla base del know-how legato alla progettazione di sistemi mucoadesivi capaci di aderire alle membrane mucose per lunghi periodi di tempo, è nata l'idea di estendere i rilevanti risultati dei sistemi transdermici, adatti all'applicazione esterna, a sistemi veicolati da agenti mucoadesivi per il rilascio del farmaco per via interna locale. Questi sistemi mucoadesivi devono aderire alle membrane mucose per il tempo necessario a liberare il loro contenuto di farmaco con un processo lento e graduale.
Gli sviluppi tecnologici derivati da questi studi, hanno portato a nuove formulazioni che grazie ad agenti in grado di favorire e accelerare la dissoluzione del farmaco all'interno della cavità orale, sono adatte a quei pazienti che possono avere difficoltà nel deglutire compresse o liquidi.
I materiali bioadesivi sono generalmente costituiti da polimeri che aderiscono alle superfici bagnate; questo significa che hanno anche la capacità di aderire alle membrane mucose nel corpo, per quanto sia spesso difficile far attaccare le cose alle superfici bagnate. In effetti, alcuni di questi materiali sono attivati soltanto una volta bagnati ed il vantaggio che offrono, in campo medico, è nella produzione di nuovi sistemi di trasporto dei farmaci, che possono essere formulati per rimanere più a lungo nelle zone necessarie e quindi possono essere molto più efficaci.
Il processo di mucoadesione coinvolge la formazione di un intimo e stretto contatto fra la superficie mucosa e le catene polimeriche del sistema mucoadesivo. La disidratazione della superficie mucosa, seguita dalla formazione di un reticolato di legami chimici secondari (in particolare, legami idrogeno) fra queste due superfici, è di importanza basilare.
I polimeri con caratteristiche mucoadesive, sono macromolecole idrofile naturali o sintetiche, che generalmente contengono gruppi idrossili o carbossilici. Questi gruppi favoriscono la formazione di legami idrogeno con le superfici mucose. I polimeri anionici si sono dimostrati i candidati migliori per la mucoadesività. Questi comprendono la famiglia di Carbopol, così come altri polimeri quali la cellulosa carbossimetilica e la gomma adragante. La mucoadesività di polimeri non ionici, quali l'idrossipropilmetilcellulosa e la metilcellulosa, presenta caratteristiche di resistenza molto inferiori rispetto ai polimeri anionici.
Le formulazioni adesive devono anche essere caratterizzate da un efficace sistema di rilascio del farmaco e per raggiungere questo scopo, oltre ai parametri fisiologici, devono essere esaminate le varie formulazioni possibili. Infatti, per quanto riguarda il rilascio del farmaco da parte dei sistemi mucoadesivi, sebbene gli studi sull'effetto di vari additivi sulle caratteristiche adesive dei polimeri mucoadesivi e delle loro formulazioni siano relativamente pochi e limitati, è certo che l'uso dei comuni eccipienti per tavolette, come pure altri additivi di formulazione, possono influenzare le prestazioni dei polimeri mucoadesivi. Trascurare l'effetto della presenza di questi additivi di formulazione sulla resistenza e sulla durata di adesione di un sistema mucoadesivo potrebbe dimostrarsi critico per l'efficacia ed il tempo di tenuta in vivo.
Gli agenti tensioattivi sono fra gli additivi più ampiamente usati nelle formulazioni farmaceutiche e sono usati per vari scopi: migliorare la solubilità ed il tasso di dissoluzione dei farmaci presenti all'interno delle formulazioni, uniformare la completa dispersione delle particelle presenti in una formulazione, offrire una buona bagnabilità delle particelle solide, una buona stabilità delle formulazioni farmaceutiche, un'attività antibatterica, un effetto detergente, ecc. Tuttavia, l'incorporazione di agenti tensioattivi all'interno delle formulazioni mucoadesive o persino la loro presenza naturale nell'ambiente fisiologico che circonda il sistema mucoadesivo potrebbe influenzare la loro capacità adesiva.
Malgrado il loro potenziale effetto sulle caratteristiche delle formulazioni mucoadesive, sono disponibili pochi studi a proposito dell'influenza dei tensioattivi.
1 Sajadi-Tabassi SA, Martin GP and Marriott C. The effects of polysorbate surfactants on the structure of mucus glycoproteins. DARU (2001) 9: 6-11
2Lehr CM, Bouwstra JA, Bodde HE and Junginger HE. A surface energy analysis of mucoadhesion: contact angle measurements on polycarbophil and pig intestinal mucosa in physiologically relevant fluids. Pharm. Res. (1992) 9: 70-75
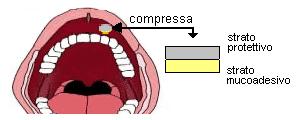 La compressa, formulata per assicurare un rilascio controllato di benzocaina (20 mg) per un periodo di 8 ore, è composta da uno strato mucoadesivo da applicare direttamente sulla gengiva alla quale rimane adesa e da uno strato protettivo per prevenire la perdita di farmaco nel cavo orale.
La compressa, formulata per assicurare un rilascio controllato di benzocaina (20 mg) per un periodo di 8 ore, è composta da uno strato mucoadesivo da applicare direttamente sulla gengiva alla quale rimane adesa e da uno strato protettivo per prevenire la perdita di farmaco nel cavo orale.
Singla AK, Chawla M and Singh A. Potential applications of carbomer in oral mucoadhesive controlled drug delivery system: a review. Drug Dev. Ind. Pharm. (2000) 26: 913-924
Jain AC, Aungst BJ and Adeyeye MC. Development and in vivo evaluation of buccal tablets prepared using danazol-sulfobutylether 7 beta-cyclodextrin (SBE 7) complexes. J. Pharm. Sci. (2002) 91: 1659-1668
rilascio oftalmico: sistemi basati sul chitosano per migliorare la ritenzione e la biodistribuzione di farmaci applicati topicamente sull'occhio si sono dimostrati di sicura efficacia. Oltre alla bassa tossicità e buona tolleranza oculare, il chitosano oltre ad interessanti caratteristiche chimico-fisiche che lo rendono un materiale d'elezione per la progettazione di formulazioni oculari di rilascio del farmaco, presenta un comportamento biologico favorevole per bioadesività ed aumento delle proprietà di permeabilità
Sono state preparate varie formulazioni come i gel di chitosano, sistemi colloidali rivestiti con chitosano e nanoparticelle di chitosano. I risultati finora ottenuti hanno fornito la prova del potenziale offerto dai gel di chitosano per l'aumento ed il prolungamento della permanenza dei farmaci sulla superficie dell'occhio; i sistemi colloidali a base di chitosano si sono dimostrati capaci di funzionare come veicolatori transmucosali del farmaco, sia facilitanti il trasporto dei farmaci all'occhio interno (sistemi colloidali chitosano-rivestiti che contengono indometacina) o la loro accumulazione nell'epitelio corneale/congiuntivale (nanoparticelle di chitosano che contengono ciclosporina). Le microparticelle farmaco-carrier (microsfere) sembrano un promettente mezzo di somministrazione dell'aciclovir nell'occhio.
rilascio nasale: la cavità nasale svolge importanti funzioni protettive all'interno del sistema respiratorio in quanto filtra, riscalda ed umidifica l'aria inalata. Le gocce inalate o le particelle vengono vengono intrappolate dai peli nel vestibolo nasale o dallo strato mucoso nella cavità principale, che gradualmente le riporta nel retrogola e giù nel tratto gastrointestinale.
Lo strato sottostante della membrana nasale è altamente vascolarizzato, e la cavità nasale offre un'ampia superficie rapidamente accessibile per l'assorbimento dei farmaci per la presenza dei turbinati nasali. Per conseguenza, farmaci lipofili a basso peso molecolare, come propanololo, progesterone e testosterone, sono ben assorbiti nella cavità nasale. Questi farmaci possono raggiungere la circolazione entro pochi minuti dalla somministrazione, giacché il sangue venoso passa dal naso alla circolazione sistemica. Le curve plasmatiche e la biodiponibilità ottenute per tali composti sono spesso confrontabili a quelli ottenuti con una iniezione endovenosa. Infatti, molti farmaci che sono somministrati per via nasale sono spesso assorbiti più efficacemente di quelli per via orale, con una più rapida comparsa dell'effetto.
La mucosa nasale costituisce il luogo ideale per i sistemi bioadesivi di rilascio dei farmaci per il trattamento di riniti allergiche. La biodisponibilità ed il tempo di ritenzione dei farmaci che sono somministrati per via nasale possono essere aumentati dai sistemi bioadesivi di rilascio. I sistemi di rilascio con chitosano (quali le microsfere) hanno la capacità di aumentare il tempo di permanenza delle formulazioni del farmaco nella cavità nasale, e ciò costituisce il potenziale per migliorare la medicazione sistemica.
La somministrazione endonasale di insulina in polvere di chitosano, nelle pecore, si è dimostrata una efficace formulazione di rilascio
Sono stati descritti anche differenti tipi di vaccini nasali che includono la tossina del colera, microsfere, nanoparticelle, liposomi, virus attenuati e cellule, e proteine esterne della membrana (proteosomi). Le formulazioni nasali inducono risposte significative di IgG seriche, simili ai livelli secretivi di IgA e superiori a quelli indotto tramite una gestione parenterale del vaccino.
 pubblicità del sistema ClindesseTM |
rilascio nel colon: il chitosano è stato usato nelle formulazioni orali per fornire il rilascio continuo dei farmaci. Recentemente è stato trovato che il chitosano è degradato dalla microflora presente nel colon. Di conseguenza, questo composto potrebbe essere promettente per il rilascio di farmaci colon specifici. Il chitosano è stato combinato esclusivamente con le anidridi succiniche e ftaliche. I polimeri semisintetici risultanti sono stati sperimentati per sistemi di rilascio orale del farmaco. I sistemi per il rilascio contenenti acetaminofene (paracetamolo), mesalazina (5-ASA), sodio diclofenac e insulina sono stati studiata e mostrato risultati soddisfacenti.
Con l'aggettivo "delitescente", sono indicate le compresse a rapida disgregazione (fast disintegrating tablets) il cui interesse è confermato dai numerosi farmaci introdotti sul mercato.
I recenti sviluppi tecnologici hanno presentato le alternative possibili di dosaggio per i pazienti che possono avere difficoltà nel deglutire compresse o liquidi. Le compresse o capsule tradizionali, sono somministrate con mezzo bicchiere d'acqua che può essere inadatto per alcuni pazienti. Per esempio, un paziente molto anziano non può deglutire una dose quotidiana di medicinale; un bambino con allergie può usare una formulazione alternativa ad uno sciroppo antistaminico; un paziente schizofrenico sottoposto a trattamento può nascondere una compressa o capsula convenzionale sotto la lingua per evitare la sua dose quotidiana di antipsicotico; una donna sottoposta a radioterapia per il cancro al seno può essere troppo nauseata per deglutire il suo H2-bloccante. Le compresse delitescenti (FDDTs , Fast-dissolving/disintegrating tablets) sono una forma farmaceutica ottimale per tutti questi pazienti.
L'assorbimento già nel cavo orale abbrevia la comparsa dell'effetto terapeutico (importante nel caso di antinfiammatori, analgesici e antinevralgici) e riduce l'effetto di primo passaggio nel fegato, con conseguente aumento della biodisponibilità.
Le compresse delitescenti si disaggregano e si dissolvono velocemente nella saliva senza la necessità dell'acqua. Alcune compresse progettate per dissolversi nella saliva in pochi secondi, sono propriamente fast-dissolving; altre contengono agenti finalizzati a migliorare la velocità di disaggregazione della capsula nella cavità orale e sono più appropriatamente definite compresse fast-disintegranting in quanto possono richiedere fino a un minuto per disaggregarsi completamente.
Le compresse delitescenti, come forma farmaceutica, hanno parecchie caratteristiche che le distinguono dalle dalle forme di dosaggio più tradizionali. Di importanza critica è il mascheramento del gusto per l'allestimento di una preparazione accettabile. Le compresse tradizionali generalmente non prevedono il mascheramento del gusto perché si tratta di formulazioni che si dissolvono dopo aver rapidamente attraversato la cavità orale. Molte sospensioni orali, sciroppi e compresse masticabili contengono semplicemente aromi, zucchero ed altri dolcificanti per contrastare il gusto amaro del farmaco; però, questi mezzi non sono sempre sufficienti per mascherare molti farmaci amari. La maggior parte delle tecnologie per compresse delitescenti comprendono un unica forma di mascheramento del gusto ottenuto principalmente con il rivestimento spray delle particelle.

La maggior parte delle compresse a rivestimento gastroenterico sono formulate come sistema singolo; queste hanno piccole dimensioni ma presentano il rischio che il rivestimento enterico possa danneggiarsi durante lo svuoatamento gastrico. Il farmaco può così essere esposto agli acidi che possono influenzare negativamente l'assorbimento.
 |
Pearlitol®200SD mannitolo spray-dried, poroso, struttura pop-corn simile, alta comprimibilità, eccellente scorrevolezza, rapida disintegrazione e bassa sensibilità lubrificante |
 |
Pearlitol®300DC mannitolo struttura estrusa e strutturata, alta densità di massa, sensazione di cremosità |
 |
Pearlitor®160C mannitolo polvere cristallina, dimensione media delle particelle 160 mm. Ideale per granulazione a umido. |
L'intervallo più ampio spazia tra le tavolette e le forme iniettive:
Pearlitol® 25C, 50C e 160C, per granulazione ad umido;
Pearlitol® 100SD e 200SD, spray dried, natura granulare con strettissima distribuzione delle particelle, eccellente compressibilità e rapida dissoluzione;
Pearlitol® 300DC, 400DC e 500DC producono un sensazione cremosa. Pearlitol® PF per preoparazioni iniettabili.
Il lansoprazolo (antiulcera inibitore della pompa protonica) è disponibile in capsule per somministrazione orale con acqua. Le capsule contengono una formulazione di lansopazolo in granuli con un rivestimento gastroenterico che protegge il principio attivo - sensibile all'ambiente acido - mentre attraversa lo stomaco. Lo strato protettivo si dissolve nell'ambiente intestinale dove il lansoprazolo è assorbito.
Poiché una piccola fessurazione o imperfezione nel rivestimento di una singola unità gastroresistente può vanificare l'intera dose, sono stati sviluppati sistemi ad unità multiple per superare questo problema. Tipiche forme farmaceutiche comprendono capsule e compresse contenenti granuli con rivestimento gastroenterico. I granuli verosimilmente sono meno sensibili allo svuotamento gastrico grazie alle loro piccole dimensioni; inoltre, eventuali danni a qualche granulo non hanno effetti sull'intera dose. Comunque, capsule e compresse possono essere considerate forme farmaceutiche relativamente grandi. La forma litescente contiene granuli del diametro fino ad un terzo inferiore a quello dei granuli comuni (d = 330 mm).
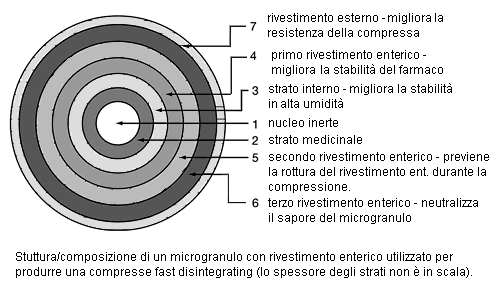
Il lansoprazolo3 è è stato il primo antiulcera inibitore della pompa protonica disponibile come sistema delitescente: una compressa per disaggregazione orale in una nuova formula ad elevata compliance perché facile da deglutire ed assumibile per via orale con o senza acqua. E' stata progettata per fornire una forma di dosaggio alternativa nella prescrivibilità del lansoprazolo, mantenendo lo stesso dosaggio delle capsule.
I granuli contenuti nelle capsule di lansoprazolo hanno un nucleo, uno strato del lansoprazolo ed un rivestimento gastroenterico; invece, ogni microgranulo della compressa delitescente ha diametro inferiore e contiene sei strati (v. fig. sopra). Lo strato attivo del lansoprazolo riveste un nucleo inerte, seguìto da uno strato inerte di rivestimento interno che migliora la stabilità verso l'alta umidità. Tre strati gastroeneterici ricoprenti impediscono la dissoluzione nello stomaco, migliorano la stabilità, riducono danni durante la compressione e neutralizzano il gusto del microgranulo. Uno strato ricoprente migliora la durezza durante il processo di compressione per realizzare la formulazione finale.
3Tabata T, Kashihara T, Hirai S, Kitanori N, Toguchi H: Effect of gastric pH on the absorption of a new antiulcer drug (lansoprazole) in the beagle dog. J Biopharm Sci 1991;2:319-328
| 8 | |||||||||
Marcello Guidotti, copyright 2007
questa pagina può essere riprodotta su qualsiasi supporto o rivista purché sia citata la fonte e l'indirizzo di questo sito (ai sensi degli artt. 2575 e 2576 cc. Legislazione sul diritto d'autore). Le fotografie sono tratte da siti web e sono, o possono ritenersi, di pubblico dominio purché utilizzate senza fini di lucro. Le immagini di prodotti presenti nel sito hanno unicamente valenza esemplificativa oltre che, eventualmente, illustrare messaggi fuorvianti e non vi è alcun richiamo diretto o indiretto alla loro qualità e/o efficacia il cui controllo è affidato alle autorità regolamentatorie.