polimorfismo
Una fase solida cristallina può organizzarsi in un reticolo cristallino in modo diverso, dando luogo a forme cristalline dette polimorfe. Circa i 2/3 delle sostanze organiche presentano il fenomeno del polimorfismo: per esempio il sulfatiazolo ha 4-5 polimorfi, il progesterone ne ha 5, la nicotinamide 4, ecc.
Le varie forme cristalline differiscono per l'attività termodinamica e sono considerate polimorfe le forme che hanno elevata attività termodinamica. Le differenti forme cristalline possono provocare comportamenti diversi per l'assorbimento, la fusione, la solubilità, ecc. E' quindi prevedibile che una forma cristallina di un certo tipo possa influenzare l'attività di un farmaco nell'organismo. Ovviamente ciò si riferisce alle forme farmaceutiche solide, ma può interessare anche le soluzioni, soprattutto quelle sature, in quanto, per esempio, per una variazione di temperatura, queste possono produrre precipitati polimorfi poco solubili rallentando così l'assorbimento.
Le cause del differente arrangiamento della struttura cristallina, possono essere dovute a:
- forme di risonanza;
- libera rotazione attorno a legami semplici;
- interazioni tra molecole dello stesso tipo;
- presenza del solvente (in genere, la forma anidra si solubilizza più facilmente).
Per fissare le idee, è utile fare riferimento alla tabella seguente, dove sono riportate le forme polimorfe del cortisone-acetato. La forma 1 è stata la prima ad essere scoperta ed è anche la più stabile avendo attività termodinamica minore; le altre forme sono metastabili.
| tipo |
p.f. ºC |
aspetto |
sistema |
densità [g/cm3] |
molecole per cella |
stato di idratazione |
| 1 |
241-245 |
aghi |
monoclino |
1,25 |
6 |
anidro |
| 2 |
235-238 |
scaglie |
ortorombico |
1,21 |
4 |
anidro |
| 3 |
233-251 |
prismi |
ortorombico |
1,21 |
4 |
anidro |
| 4 |
237-245 |
prismi |
ortorombico |
1,25 |
4 |
bi-idrato |
| 5 |
238-242 |
aghi |
monoclino |
1,25 |
2 |
bi-idrato |
La tabella seguente riporta la percentuale di polimorfi per alcune sostanze di interesse farmaceutico.
| farmaci |
composti esaminati |
% di polimorfi |
% di polimorfi instabili
o metastabili |
| steroidi con p.f. < 210 ºC |
48 |
67% |
17% |
| sulfamidici |
40 |
40% |
23% |
| barbiturici |
38 |
63% |
11% |
Per studiare il polimorfismo di una sostanza, è necessario esaminare le seguenti questioni:
- numero di forme cristalline possibili ed intervallo di temperatura in cui sono stabili;
- esistenza di uno stato non cristallino (amorfo) e sua possibile utilizzazione in una forma farmaceutica;
- esistenza di forme metastabili e possibilità di stabilizzarle;
- solubilità di ciascuna forma e studio della possibilità di ottenere cristalli puri di ciascuna forma;
- qualora la forma più solubile sia metastabile, occorre valutare se questa si mantiene tale anche dopo particolari processi di fabbricazione (micronizzazione, compressione, ecc.);
- studio della reattività con gli altri componenti la forma farmaceutica.
Le strutture polimorfe vengono studiate ricorrendo a varie tecniche, cui accenniamo solo per completezza, senza entrare nei dettagli:
- diffrazione da raggi X;
- microscopia ottica (con luce polarizzata e possibilità di riscaldamento a varie temperature) ed elettronica;
- spettroscopia I.R.;
- analisi termica differenziale o calorimetria differenziale;
- dilatometria (sfrutta le differenze di densità fra le varie forme cristalline).
problemi legati al polimorfismo
Un problema oggi noto riguarda i medicinali copia, prodotti prima dell'introduzione della copertura brevettuale per i farmaci (1978). Prima di allora, infatti, qualsiasi Azienda farmaceutica poteva copiare e commercializzare un prodotto farmaceutico giudicato commercialmente interessante. Tuttavia, per ottenere l'AIC, non era necessario fornire prove di bioequivalenza in quanto questo concetto, di là a venire, era implicito nell'utilizzazione dello stesso principio attivo. Ma nella composizione di un medicinale A, l'identità del principio attivo con il medicinale B, non è sufficiente per garantire che i due medicinali producano gli stessi risultati in termini di efficacia ed effetti collaterali. Infatti, eccipienti ed eventuali polimorfi del principio attivo possono modificare la bioequivalenza di una data formulazione.
Gli esempi che seguono offrono una breve panoramica per comprendere le problematiche associate al polimorfismo.
La Novobiocina è un antibiotico somministrato come polvere micronizzata per via orale; si presenta in forma cristallina o amorfa. Esistono anche i sali di Ca e Na (poco stabile) che ne aumentano la solubilità.
Esaminando i livelli ematici ottenuti con la somministrazione del sale sodico e delle forme cristallina e amorfa (tutte micronizzate), si è visto che la forma amorfa è circa 10 volte più solubile della forma cristallina (che difficilmente supera la d.m.e., dose minima efficace) e presenta un'efficacia quasi pari al sale sodico con il vantaggio di una maggior stabilità. Tuttavia, la forma amorfa, come tutte le forme metastabili, tende a trasformarsi (per cause esterne quali temperatura e pressione) nella forma cristallina stabile. Nel caso della Novobiocina, questa trasformazione avviene in pochi mesi e ridurrebbe la durata della forma farmaceutica; sicché si deve ricorrere a particolari accorgimenti per ritardare questo processo. Così, ad esempio, si usano sostanze ispessenti che aumentano la viscosità e quindi la stabilità; diversamente, si possono cercare sostanze la cui aggiunta impedisce o rallenta la trasformazione.
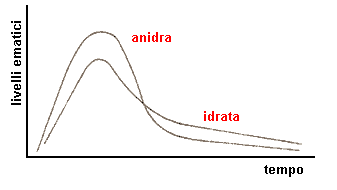 L'Ampicillina si può trovare in due forme: anidra e idrata; la prima, presenta una solubilità maggiore del 20% rispetto alla forma anidra, ed ha una maggior velocità di dissoluzione.
L'Ampicillina si può trovare in due forme: anidra e idrata; la prima, presenta una solubilità maggiore del 20% rispetto alla forma anidra, ed ha una maggior velocità di dissoluzione.
L'andamento dei livelli ematici in funzione del tempo è rappresentato nel grafico a destra (non in scala). E' importante tener conto del fatto che, a parità di dose, l'area sottesa dalle due curve è uguale per entrambe le forme in quanto i livelli ematici tendono a zero in tempi diversi; ne segue che miscelando opportunamente la forma anidra e quella idrata, è possibile ottenere una composizione caratterizzata da un buon livello ematico, una più rapida comparsa dell'effetto terapeutico ed una maggior durata d'azione.
Il Cloramfenicolo palmitato può presentarsi in 4 forme di cui tre cristalline (A, B, C) ed una amorfa (D); le prime due sono più frequenti, le altre debbono essere preparate appositamente. Sul grafico a destra (non in scala), sono riportati i livelli ematici ottenuti con la somministrazione delle 5 combinazioni seguenti:
1- costituita da solo polimorfo A
2- costituita dal 25% di B e dal 75% di A
3- costituita dal 50% di B e dal 50% di A
4- costituita dal 75% di B e dal 25% di A
5- costituita da solo polimorfo B |
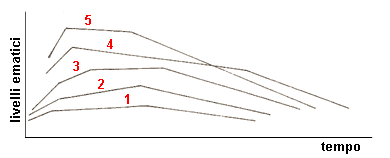 |
Il polimorfo B (5) è quello maggiormente attivo, viceversa A (1) non raggiunge un livello terapeuticamente efficace. In particolare, la differente efficacia è dovuta essenzialmente alla maggior solubilità di B, mentre A è così poco solubile che gli enzimi presenti nell'organismo non riescono ad idrolizzarlo liberando la base da assorbire. D'altra parte, B è metastabile e si trasforma lentamente in A limitando l'efficacia del prodotto. La F.U. X ed. considera (solo in questo caso) il fenomeno del polimorfismo prescrivendo che la percentuale del polimorfo A, presente in una forma farmaceutica non sia superiore al 10%
L'Insulina (secondo F.U. X ed.) è disponibile in varie forme iniettabili:
Insulina Zinco amorfa sospensione iniettabile (detta anche semilenta). E' una sospensione neutra sterile di insulina (bovina o porcina) complessata con un sale di zinco appropriato; l'insulina è in forma insolubile in acqua.
Insulina Zinco cristallina sospensione iniettabile (detta anche ultralenta). E' una sospensione neutra sterile di insulina bovina, porcina o di insulina umana complessata con un sale di zinco appropriato; l'insulina è in forma di cristalli insolubili in acqua.
Miscelando 3 parti di insulina semilenta con 7 parti della ultralenta, si ottiene un'insulina lenta (insulina zinco sospensione iniettabile) che presenta rapida comparsa dell'azione e buona durata. La differente origine dei due componenti comporta una definzione più ampia: è una sospensione neutra sterile di insulina bovina, porcina, o di insulina bovina e porcina o di insulina umana complessata con un sale di zinco appropriato; l'insulina è in forma insolubile in acqua.
Non è considerata l'insulina Lispro® in quanto essendo un'insulina umana modificata con la tecnica del DNA ricombinante (la sequenza di due aminoacidi nella catena B della molecola dell'insulina è stata modificata, cioè la Prolina e la Lisina, sono stati posposti nella sequenza Lisina-Prolina che costituisce fra l'altro la ragione del nome LIS-PRO) è un prodotto che non costituisce un problema di tecnologia farmaceutica.
Marcello Guidotti, copyright 2003, 2006
questa pagina può essere riprodotta su qualsiasi supporto o rivista purché sia citata la fonte e l'indirizzo di questo sito (ai sensi degli artt. 2575 e 2576 cc. Legislazione sul diritto d'autore). Le fotografie sono tratte da siti web e sono, o possono ritenersi, di pubblico dominio purché utilizzate senza fini di lucro. Le immagini di prodotti presenti nel sito hanno unicamente valenza esemplificativa oltre che, eventualmente, illustrare messaggi fuorvianti e non vi è alcun richiamo diretto o indiretto alla loro qualità e/o efficacia il cui controllo è affidato alle autorità regolamentatorie.
 L'Ampicillina si può trovare in due forme: anidra e idrata; la prima, presenta una solubilità maggiore del 20% rispetto alla forma anidra, ed ha una maggior velocità di dissoluzione.
L'Ampicillina si può trovare in due forme: anidra e idrata; la prima, presenta una solubilità maggiore del 20% rispetto alla forma anidra, ed ha una maggior velocità di dissoluzione.