generalità sul controllo di qualità
Durante la produzione delle formulazioni farmaceutiche, si possono presentare dei difetti per evitare i quali sono previsti alcuni controlli fondamentali: uniformità di massa; tempo di disaggregazione; velocità di dissoluzione.
A titolo esemplificativo, esaminiamo alcuni controlli previsti per le compresse e le capsule, rimandando alla consultazione della FU per le altre forme farmaceutiche.
uniformità di massa (compresse non rivestite e rivestite con film)
La massa delle singole compresse può essere influenzata dall'umidità delle polveri impiegate (in quanto ne limita lo scorrimento), da cattiva omogeneità del granulato, da deformazione dei punzoni, ecc. Per controllare l'uniformità di massa, la F.U. stabilisce le seguenti percentuali di tolleranza:
| massa media |
deviazione percentuale |
| 250 mg o maggiore |
5 |
| oltre 80 e meno di 250 mg |
7.5 |
| 80 mg o inferiore |
10 |
Per scarto o deviazione percentuale, si intende la differenza, in valore assoluto, tra la massa media e la massa delle sinole unità rapportata a 100.
Il controllo viene eseguito in questo modo: si pesano singolarmente 20 compresse prelevate a caso da un lotto di produzione e si compila una tabella con i risultati delle pesate dei quali si calcola la massa media.
Il saggio richiede che 18 compresse appartenenti al lotto di 20 unità devono rientrare nella deviazione percentuale; le restanti 2 compresse non devono comunque superare il doppio della deviazione percentuale.
| massa unitaria |
scarto |
risultato |
| 6 x 119,95 |
0,02 |
accettato |
| 4 x 119,88 |
0,09 |
respinto |
| 3 x 120,04 |
0,07 |
accettato |
| 7 x 120,01 |
0,04 |
accettato |
esempio: un campione di 20 compresse è formato da unità aventi le singole masse riportate in tabella (per semplicità, si è supposto le compresse abbiano masse raggruppabili in 4 fasce).
La massa media è: (6 × 119,95 + 4 × 119,88 + 3 × 120,04 + 7 × 120,01)/ 20 = 119,970 mg
In questo caso (oltre 80 e meno di 250 mg), il valore di deviazione da utilizzare è 7.5
Dai dati in tabella, risulta che 4 compresse superano il valore minimo e quindi il lotto da cui sono state campionate le compresse deve essere respinto. Se le compresse di massa non conforme fossero state solo due, allora il lotto sarebbe stato accettato in quanto il limite di deviazione rientra nel doppio della deviazione percentuale.
Per le compresse rivestite, la F.U. richiede il saggio dell'uniformità di massa solo per i nuclei, e non per le compresse in toto, in quanto le variazioni di massa del rivestimento possono essere notevoli.
Le massime variazioni di massa consentite per il contenuto delle capsule opercolate, sono ± 5 (meno di 300 mg) e ± 10 (300 mg o più).
tempo di disaggregazione
Il saggio previsto dalla FU permette di determinare se le compresse o le capsule si disaggregano entro il tempo prescritto quando vengono poste in un mezzo liquido con specifiche condizioni sperimentali.
Il tempo di disaggregazione può dipendere da un'eccessiva pressione dei punzoni, da un'eccessiva quantità di legante, oppure dalla presenza di un lubrificante. Per questo controllo, si impiega un contenitore del tipo riportato in figura (la FU ne specifica puntualmente caratteristiche e le dimensioni a seconda della forma farmaceutica), il quale, con un apposito meccanismo, viene alternativamente abbassato e sollevato (per simulare i movimenti peristaltici dello stomaco) all'interno di una soluzione la cui composizione è formulata a seconda del tipo di compressa (confetti, compresse gatroresistenti, ecc.).
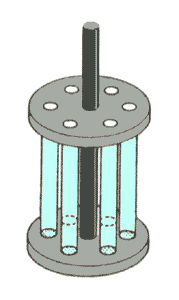
- compresse: inserite nei cilindri alla temperatura compresa fra 36-38 ºC, dovranno disaggregarsi entro il tempo prescritto (tipicamente 15').
- compresse rivestite: si utilizza ancóra il dispositivo usato per le compresse, ma il tempo massimo di disaggregazione è 1 h (la prima prova si effettua in acqua, e se le compresse non dovessero disaggregarsi, si ripete in soluzione cloridrica (0.1 M) fissando in 1 h il limite di tempo).
- compresse o confetti gastroresistenti: si dovrà fare prima una prova in soluzione di HCl (dove non si dovrà avere disaggregazione per almeno 2h) e poi una seconda prova in ambiente tamponato a pH 6.8 dove si dovrà avere disaggregazione in 1 h.
- capsule di gelatina molle e dura: per i due tipi di capsule è molto importante il controllo della disaggregabilità che viene effettuato con lo stesso apparecchio utilizzato per le compresse. Le capsule, immerse in un succo gastrico artificiale, devono dimostrare gastroresistenza non aprendosi per 0.5 o 1 h, a seconda delle prescrizioni. Sùbito dopo, immergendo le capsule così trattate in succo enterico artificiale, si devono distruggere in 30 minuti.
 |
La disaggregazione si intende raggiunta quando:
- nessun residuo rimane sulla rete del cestello, o
- se c'è un residuo, è costituito da una massa molle, senza nucleo palpabile, duro, non inumidito, o
- rimangono solo frammenti del rivestimento (compresse) o solo frammenti dell'involucro (capsule).
uniformità di contenuto
Si può verificare che le compresse, pur rientrando nei limiti dell'umiformità di massa, abbiano un contenuto in principio attivo non costante (per es., dovuto alla cattiva miscelazione del materiale di partenza o alla segregazione). Questo problema è tanto più importante quanto più il farmaco è attivo. Per le modalità di esecuzione dei saggi si rimanda alla F.U.
velocità di dissoluzione
E' stato molto raramente dimostrato che esiste una correlazione precisa tra il test di dissoluzione e la biodisponibilità, anche se la velocità di dissoluzione rappresenta una delle fasi di assorbimento di un prodotto ed è molto utile per il controllo della costanza dei vari lotti non essendo pensabile controllarne la biodisponibilità.
Il dispositivo più diffuso è costituito da un recipiente chiuso dotato di un sistema di immissione e prelievo del liquido e di un termometro.
All'interno del recipiente è posto un cestello a maglie che ruota con velocità costante (20-200 giri/minuto) in un liquido opportuno: nel caso di normali compresse si usa un liquido gastrico artificiale (costituito da pepsina, HCl, NaCl, acqua a pH acido), mentre per le compresse gastroresistenti si usa un liquido intestinale artificiale (pancreatina, NaHPO, NaOH, acqua con pH quasi neutro). Dopo l'inizio della prova, ad intervalli di tempo regolari, si prelevano campioni del liquido dosandovi quantitativamente il farmaco. Le compresse ricoperte hanno ovviamente minor velocità di rilascio del principio attivo.
Anche per le capsule, come per le compresse, si effettua anche il controllo della velocità di dissoluzione dei princìpi attivi.
altri controlli
Le officine di produzione, effettuano altri controlli a garanzia dell'immagine del produttore:
- dimensioni: in conseguenza della confettatura, alcune compresse possono risultare deformate o con dimensioni fuori dello standard di produzione;
- perdita di rivestimento può dipendere da carenza di aggregante o da eccessiva compressione che provoca successivamente una tendenza a riespandersi, da un eccesso di polveri fini, dalla corrosione dello stampo, dall'umidità del granulato;
- presenza di macchie: dovuta generalmente alla migrazione del colorante;
- stabilità della forma farmaceutica: comprene una serie di controlli che vanno dalla sterilità al tempo di semivita.
Marcello Guidotti, copyright 2003
questa pagina può essere riprodotta su qualsiasi supporto o rivista purché sia citata la fonte e l'indirizzo di questo sito (ai sensi degli artt. 2575 e 2576 cc. Legislazione sul diritto d'autore). Le fotografie sono tratte da siti web e costituiscono materiale pubblicitario, oppure sono, o possono ritenersi, di pubblico dominio purché utilizzate senza fini di lucro.


