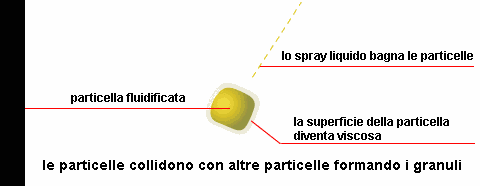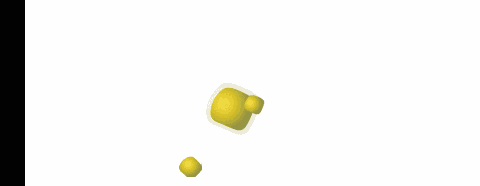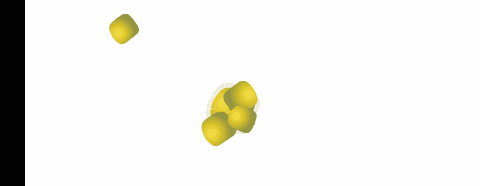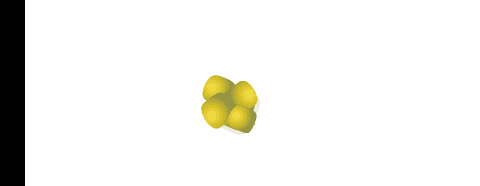



Vi sono due differenti modalità di granulazione a letto fluido: in fase secca o bagnata. Nella granulazione in fase secca, le particelle richiedono solo una leggera bagnatura per diventare collose e riunirsi l'una con l'altra. La soluzione granulante è applicata ad una velocità minore o uguale alla velocità di evaporazione, in modo che le particelle rimangano secche durante l'intero processo.
Nella granulazione in fase umida, le particelle richiedono un maggior cospargimento prima che diventino abbastanza collose da potersi riunire l'una con l'altra. La soluzione granulante è applicata ad una velocità maggiore di quella di evaporazione finché le particelle raggiungono l'umidità sufficiente per la granulazione. Le caratteristiche delle particelle bagnate ed il tipo di soluzione granulante usato, determinano quale debba essere il procedimento più appropriato. Mentre la fase secca è più comune, la fase umida permette di ottenere prodotti pù densi.
L'animazione, parzialmente convertita da Flash e adattata in gif animata, è stata tratta dal sito: www.vectorcorporation.com/flash/fluidbed.htm
Copyright ©2000 Fluid Air Incorporated. All rights reserved
I granulati effervescenti contengono componenti a reazione acida e carbonati o bicarbonati in grado di reagire rapidamente, in presenza di acqua, liberando anidride carbonica.
Un comune metodo di preparazione prevede bicarbonato di sodio e acido citrico (di cui il 20-25% monoidrato), unitamente ad altri componenti miscelati e riscaldati fino alla liberazione di acqua di cristallizzazione dell'acido citrico che agisce da agente granulante. In questo caso il contenuto riscaldamento e la limitata quantità di acqua provocano una modesta liberazione di anidride carbonica che contribuisce a rendere spugnosa la massa. Come dolcificante, si addizionano quelli previsti dalla legge.
Se per esempio si vogliono preparare 10 bustine da 5 g ciascuna in granulato effervescente contenente 500 mg di acido acetilsalicilico per bustina, le relative quantità dei componenti si calcolano come segue:

La miscela effervescente (45 g) è costituita da: acido citrico, acido tartarico (acidificante, esaltatore di sapidità), bicarbonato di sodio
Il calcolo delle quantità di acido citrico e bicarbonato da utilizzare è basato sull'equazione stechiometrica:
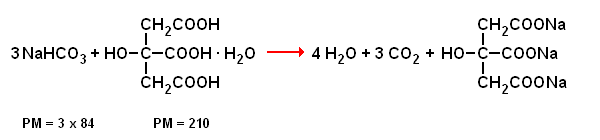
Dalla stechiometria della reazione acido citrico + bicarbonato, risulta che per 1 g di acido citrico sono necessari 1,2 g di bicarbonato (1 : 210 = x : 252).
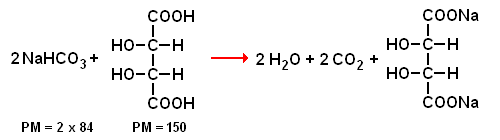
Dalla stechiometria della reazione acido tartarico + bicarbonato, risulta che per 1 g di acido tartarico sono necessari 1,12 g di bicarbonato (1 : 150 = x : 168)
| bicarbonato | ac. citrico | ac. tartarico |
| 1.2 | 1 | |
| 1.12 | 1 | |
| g di bicarbonato necessari rispettivamente per 1 g di ac. citrico e 1 g di ac. tartarico |
||
1 g ac. citrico + 1,2 g di bicarbonato + 2 ·[1 g ac. tartarico + 1,12 g di bicarbonato] = 6,4 g di miscela effervescente.
Ora, occorre calcolare le quantità di miscela effervescente necessarie per i 45 g richiesti per ogni bustina: occorrono 45/6,4 = 7 unità di miscela (acido citrico, ac. tartarico, bicarbonato). In pratica, rispettando i rapporti dei componenti abbiamo: 7 ac. citrico + 14 ac. tartarico + 24 [ = 7 · (1,2 + 2,22)] sodio bicarbonato = 45 g. A questa miscela si addizioneranno i 5 g di acido acetilsalicilico.
Uno dei problemi nella produzione dei granulati effervescenti è costituito dalla presenza di umidità sia durante la preparazione sia nel prodotto finito. Il prodotto viene protetto introducendo nel tappo del contenitore un essiccante (gel di silice, solfato di calcio anidro).

La formulazione esaminata è stechiometrica; tuttavia, per variare il gusto, e per raggiungere il volume desiderato è possibile miscelare i componenti in quantità non stechiometrica. Per es., ciascuna tavoletta di Alka-Seltzer® contiene acido acetilsalicilico 324 mg, sodio bicarbonato 1625 mg, acido citrico anidro 965 mg
L'acido citrico da solo è sufficiente per conferire un carattere frizzante all'acqua, unitamente al gusto (aspro) di limonata. Invece, addizionando l'acido tartarico - che produce sulla lingua e sul palato una sensazione di fresco accompagnata dal sapore salato del tartrato (ottenuto dalla salificazione dell'ac. tartarico) - all'acido citrico (sapore aspro), c'è un sinergismo tra i due sapori.
| sapore di riferimento | dolce | amaro | salato | aspro |
| dolce | attenuato | equilibrato | attenuato | |
| amaro | equilibrato | rinforzato | rinforzato | |
| salato | attenuato | esaltato | esaltato | |
| aspro | attenuato | rinforzato | rinforzato |
Come mostra la tabella, una possibilità da non trascurare è la sostituzione del sale con le spezie. Infatti, il salato viene esaltato dall'amaro e dall'aspro, per cui si può ridurre il sale (per le diete iposodiche), rinforzando la poca quantità usata con sostanze aspre o amare (il pepe - che costituisce una combinazione di aspro e amaro) sulle patate arrosto, oppure limone e/o aceto sull'insalata).
| 7 | ||||||||||||||
Marcello Guidotti, copyright 2003-2005-2009-2010
questa pagina può essere riprodotta su qualsiasi supporto o rivista purché sia citata la fonte e l'indirizzo di questo sito (ai sensi degli artt. 2575 e 2576 cc. Legislazione sul diritto d'autore). Le fotografie sono tratte da siti web e sono, o possono ritenersi, di pubblico dominio purché utilizzate senza fini di lucro. Le immagini di prodotti presenti nel sito hanno unicamente valenza esemplificativa oltre che, eventualmente, illustrare messaggi fuorvianti e non vi è alcun richiamo diretto o indiretto alla loro qualità e/o efficacia il cui controllo è affidato alle autorità regolamentatorie.