gel polimerici
Accanto ai sistemi dispersi caratterizzati da un comportamento sol-gel reversibile, sono sempre più diffuse le soluzioni (non dispersioni) di gel polimerici. Di séguito è proposto un elenco orientativo di quanto disponibile, unitamente ad un semplice riassunto esemplificativo delle caratteristiche fondamentali dei polimeri.
- gel da bagno, gel per modellare i capelli e tutto quello che necessiti per la cura della propria persona;
- gel protettivo e dopo sole creati per aiutare a contrastare l'invecchiamento della pelle dovuto all'esposizione prolungata al sole;
- vernici in gel;
- inchiostri in gel;
- gel repellente degli insetti;
- gel usato per fare le lenti a contatto;
- gel per il trattamento dell'occhio secco;
- gel biocompatibile per la ricostruzione di cartilagini ossee;
- gel anti dolorifico e anti infiammatorio;
- gel colorato in sostituzione del fondotinta;
- suole di gel comode per le scarpe;
- gel che assorbe 400 volte il suo peso nellacqua, usato come sostituto della terra per piante in vaso;
- cuscino a gel di silicone per la prevenzione delle piaghe da decubito.
le caratteristiche dei polimeri
I polimeri sono delle macromolecole con caratteristiche del tutto particolari, non esclusivamente correlate alle dimensioni bensì al concorrere di tre proprietà uniche che sono attribuite solo alle molecole giganti.
- reticolazione: la maggior parte dei polimeri sono polimeri lineari, cioé molecole i cui atomi sono uniti in una lunga catena. Generalmente questa catena non è rigida e dritta, ma è flessibile. Le molecole polimeriche ruotano e si piegano, torcendosi e avviluppandosi una intorno all'altra, in modo tale da formare una enorme massa aggrovigliata.
Quando un polimero viene fuso, le catene assomigliano ad un piatto di spaghetti aggrovigliati; se si cerca di prenderne uno, viene via senza problemi, ma quando i polimeri sono freddi, allo stato solido, agiscono come spaghetti freddi: cercare di tirare fuori un filo da questo groviglio è più difficile.
I polimeri solidi si comportano in modo analogo: le catene sono tutte aggrovigliate una con l'altra ed è difficile districarle. Questa è la ragione che rende particolarmente resistenti alcune plastiche, vernice, elastomeri, e compositi.
- somma delle forze intermolecolari: tutte le molecole, sia quelle piccole che i polimeri, interagiscono una con l'altra, attraendosi grazie a foze elettrostatiche. Alcune molecole vengono attratte più di altre. Le molecole polari si uniscono insieme meglio di quelle non polari.
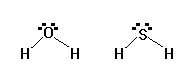 Ad esempio, l'acido solfidrico ha una struttura simile a quella dell'acqua ed ha un peso molecolare maggiore dell'acqua (32 contro 18), eppure a temperatura ambiente l'acido solfidrico è un gas e l'acqua è in fase liquida. Questo perché l'acqua è molto polare, tanto da formare legami idrogeno intermolecolari che permettono alle molecole di rimanere in fase liquida; al contrario, l'acido solfidrico non è sufficientemente polare da permettere alle sue molecole di attrarsi reciprocamente.
Ad esempio, l'acido solfidrico ha una struttura simile a quella dell'acqua ed ha un peso molecolare maggiore dell'acqua (32 contro 18), eppure a temperatura ambiente l'acido solfidrico è un gas e l'acqua è in fase liquida. Questo perché l'acqua è molto polare, tanto da formare legami idrogeno intermolecolari che permettono alle molecole di rimanere in fase liquida; al contrario, l'acido solfidrico non è sufficientemente polare da permettere alle sue molecole di attrarsi reciprocamente.
Le forze intermolecolari influenzano i polimeri proprio come le piccole molecole. Nei polimeri queste forze sono altamente combinate. Più è grande la molecola più è facile che si presentino forze intermolecolari.
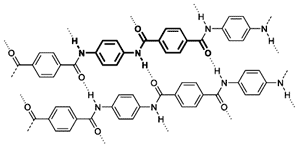 |
| Fig. 2 - struttura del kevlar®, il monomero che si ripete è in grassetto. Le fibre lineari sono connesse da legami idrogeno.
|
Anche le deboli forze di Van der Waals possono essere molto forti nel legare insieme diverse catene polimeriche; questa è un'altra ragione per cui i polimeri possono essere materiali molto resistenti. Il polietilene, ad esempio, è altamente non polare, ha solo le forze di Van der Waals ma è talmente resistente che viene utilizzato anche per produrre giubbotti antiproiettile, oggi basati sul Kevlar® (v. fig. 2), una fibra organica della famiglia delle poliammidi aromatiche, che a parità di peso è 5 volte più resistente dell'acciao).
- micromoto browniano: i polimeri si muovono molto più lentamente di quanto si muovano le piccole molecole. Un gruppo di piccole molecole si può muovere avanti e indietro molto più velocemente e in modo molto più disordinato quando le molecole non sono legate l'una all'altra; viceversa, quando le molecole sono unite in una enorme molecola, rallentano il loro movimento. Questa bassa velocità di movimento, detta micromoto browniano, fa sì che le loro soluzioni siano molto più viscose del solvente puro. La misurazione di questo cambio di viscosità viene utilizzata per stimare il peso molecolare del polimero.
 |
|
 |
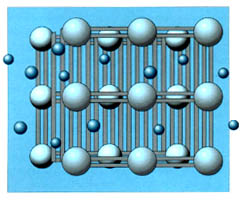
A temperature insufficienti (Fig. 3), le catene molecolari del polimero formano una superficie continua che limita la perdita di calore del corpo arrestando il trasferimento del vapore e del calore.
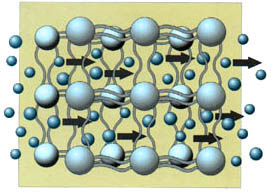
A temperature maggiori (fig. 4), i cambiamenti di configurazione molecolari formano intercapedini. Ciò permette il trasferimento di calore e del vapore da traspirazione e contribuisce ad impedire il disagio ed l'umidità all'interno dell'indumento (illustrazioni tratte dal sito: www.diaplex.com) |
Il micromoto-Browniano (o vibrazione termica), si presenta a determinati intervalli di temperatura (v. figg. 3,4) e permette alle molecole che compongono un polimero di formare fessure (micropori). Per esempio, in un indumento polimerico, queste fessure sono attivate con l'aumentare della temperatura esterna o, a basse temperature, quando la temperatura dell'indumento aumenta dopo un esercizio faticoso. Le molecole del vapore acqueo attraversano le intercapedini e sono espulse alla parte esterna. Anche il rilascio del farmaco da un sistema transdermico avviene con questo processo, e questo spiega la necessità di conservare il medicinale a temperature non superiori a 25ºC e l'avvertenza di seguire il paziente se è in stato febbrile.
interazioni tra polimeri
Quando sciogliamo un polimero in un solvente l'intera soluzione viene resa molto più viscosa in quanto i lenti polimeri ostacolano le veloci molecole di solvente che tentano di scorrere. Però, le molecole di polimero oltre ad ostacolare il movimento delle piccole molecole, le rallentano anche attraverso le forze intermolecolari. Se si verificano significative interazioni secondarie tra il polimero e le molecole del solvente, queste possono rimanere legate al polimero; in questo caso, esse si muovono più o meno insieme al polimero e, naturalmente, alla sua stessa bassa velocità.
A seconda la quantità di polimero disciolto, la soluzione può essere diluita o concentrata. Le figg. 5 e 6 mostrano le variazioni legate all'aumento di concentrazione.

| |
 |
| Fig. 5 - mancano le interazioni e le molecole sono separate tra loro |
|
Fig. 6 - le interazioni tra le molecole fanno sì che si formi un insieme unico |
La fig. 5, evidenzia l'assenza di interazioni tra catene ramificate sciolte in soluzioni diluite. Persino quando la soluzione è altamente viscosa, le catene ramificate si comportano come delle uniche entità che si muovono liberamente attraverso le molecole di solvente, senza esercitare forze di ogni tipo l'una sull'altra. Conseguentemente, nessun legame può essere stabilito tra di loro in quanto le interazioni sono praticamente inesistenti.
Nelle soluzioni concentrate, come schematizzato dalla fig. 6, la situazione è differente. All'aumentare della concentrazione, le molecole sono costrette ad avvicinarsi e l'interazione tra di loro inizia a notarsi. La somma delle forze intermolecolari diventa un fattore chiave, tanto che la viscosità (dipendente dal peso molecolare - cfr. reologia) aumenta drasticamente e la soluzione inizia a mostrare una transizione da soluzione concentrata a gel perché le catene ramificate creeranno dei legami in alcuni punti, costituendo un'unico grande gomitolo (coil) reticolato, chiamato gel macroscopico.
Le catene ramificate si legano in due modi: attraverso interazioni secondarie (valenza secondaria del gel, secondary valence gels) e attraverso legami covalenti (gel covalente, covalent gels).
- gel di valenza secondaria: le interazioni secondarie sono reversibili e interessano le differenti catene ramificate (legami intermolecolari) e le stesse catene ramificate (forze intramolecolari). La fig. 7, mostra la catena ramificata con soli legami intermolecolari (rappresentati come cerchietti ben definiti); la fig. 8, mostra due catene ramificate con sia le forza intra che intermolecolari.
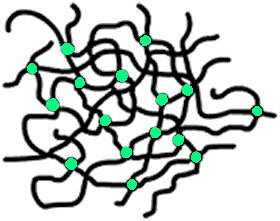 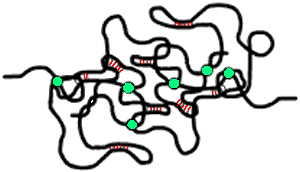
Fig. 7 (sx), Fig. 8 (dx) - legami intermolecolari ; legami inter e intramolecolari
|
Normalmente la formazione di un gel di valenza secondaria dipende da due fattori: l'intensità delle forze intermolecolari, che misura la tendenza del polimero a stabilire legami non covalenti, e la qualità del solvente.
Se consideriamo le forze intermolecolari, ci si può chiedere quale tipologia di polimeri che usano l'acqua come solvente, possa formare un gel attraverso interazioni secondarie. Un esempio comune ed immediato può essere ottenuto anche in cucina...
Tutto il necessario consiste in un budino di gelatina, conservato in frigorifero, come quello mostrato nella figura a sinistra. Se prendiamo con un cucchiaio un pò di gelatina e la mettiamo in un recipiente a bagnomaria, oppure la scaldiamo usando un forno a microonde, troviamo che gradualmente la gelatina fluidifica e diventata un liquido viscoso, poi lasciandola raffreddare, solidificherà di nuovo.
Per spiegare questo comportamento, dobbiamo riferirci alla composizione e struttura della gelatina, che è formata principalmente da collagene proteico, un polimero naturale. Questo significa che ci sono alcuni gruppi ammidici nella struttura in grado di stabilire legami idrogeno l'uno con l'altro.
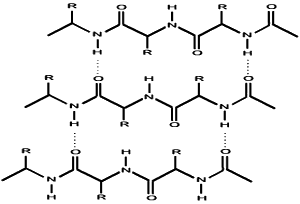
La figura sopra mostra legami non covalenti tra le catene delle proteine. Il legame idrogeno è un'interazione relativamente forte che si può rompere mediante riscaldamento.
Anche altri polimeri naturali formano gel attraverso legami secondari, come ad esempio la pectina, l'agar, e l'amido. Questa è la ragione per cui vengono usati nell'industria come addensanti, che conferiscono maggiore consistenza a molti cibi. Il PVC, pur non essendo un polimero naturale, può anch'esso formare un gel di valenza secondaria scegliendo solventi "adatti". Quando il PVC è miscelato con liquidi chiamati plastificanti crea il gel termo-reversibile (come ftalati, ad esempio), comunemente chiamato "PVC elasticizzato" con consistenza gommosa o dura come il cuoio.
A questo punto, poiché per il solvente abbiamo usato l'aggettivo "adatto", è naturale chiedersi cosa accade quando il solvente non è adatto...
Generalmente i solventi "poveri" garantiscono una incompleta solvatazione, quindi esiste un equilibrio di solvatazione e, per conseguenza, si stabiliscono prevalentemente legami intramolecolari piuttosto che intermolecolari: la densità della reticolazione è piuttosto bassa ed i legami stabiliti dalle interazioni secondarie vengono facilmente rotti.
- gel covalente: a differenza del gel di valenza secondaria che può essere rotto senza difficoltà, non esiste alcun solvente così energico da causare la rottura dei legami covalenti. Inoltre, questi tipi di legami sono resistenti anche al calore (termoindurenti reticolati), ed è proprio questo che costituisce un problema per il loro smaltimento.
Il gel covalente può essere ottenuto semplicemente facendo aumentare di volume un polimero precedentemente reticolato, scegliendo un solvente appropriato. Per esempio, la poliacrilammide è solubile in acqua, ma la poliacrilammide reticolata no: viene impiegata per realizzare lenti a contatto morbide.

Le tre proprietà discusse (reticolazione, forze intermolecolari, micromoto browniano) non sono presenti nelle dispersioni colloidali. Queste dispersioni, infatti, non sono formate da macromolecole, bensì da piccole molecole (flocculi) che si gonfiano ma rimangono separate una dall'altra, piuttosto che riunirsi in una macromolecole.
diffusione e proprietà meccaniche dei gel
I segmenti delle catene ramificate raramente possono muoversi liberamente: il loro moto dipende dalla struttura chimica del segmento, dalla concentrazione, dalla densità della catena ramificata e, ovviamente, dal grado di reticolazione. Questo movimento, ricordiamo, è chiamato moto micro-browniano. Questo è il motivo per cui il gel, sotto l'azione di una forza deformante, può reagire con una certa elasticità. Ovviamente la resistenza del gel cresce con l'aumentare del grado di reticolazione, così anche la loro durezza diventa maggiore, come per i polimeri solidi. Le proprietà dello stato solido sono solitamente mantenute quando il sistema si avvicina allo stato gel; così i polimeri duttili (cioè capaci di deformarsi prima di rompersi) si trasformano in gel duttile (es. PMMA), mentre i polimeri gommosi (es. PS) formano gel con una certa durezza.
|
polimetilmetacrilato PMMA: ottenuto per polimerizzazione dell'acido metacrilico con alcol metilico. Viene utilizzato per la produzione di lastre trasparenti, lastre per coperture, insegne luminose e per apparecchiature ottiche. Il PMMA è l'unico materiale non permeabile utilizzato per lenti a contatto; è stabile, duro, ha elevata qualità ottica, non è attaccabile da enzimi organici ed è ben tollerato dai tessuti coi quali viene a contatto. Per assenza di polarità, non assorbe acqua e lega scarsamente con le sostanze contenute nel film lacrimale, o lacrima.
polistirene PS: ottenuto dalla polimerizzazione dello stirene. Viene largamente usato nella produzione di articoli per uso domestico, grandi e piccoli elettrodomestici, giocattoli, elettronica di consumo.
|
Una questione interessante riguarda il confronto fra la resistenza meccanica dei gel ed i corpi solidi. La differenza è legata al ruolo giocato dal solvente nei sistemi polimerici: quando questi sono solidi, le catene sono abbastanza vicine le une alle altre ed il materiale può resistere bene alle deformazioni senza rompersi. Per contro, quando entrano in gioco le molecole del solvente, come nel gel, queste penetrano attraverso le catene allontanandole; quindi, con le catene separate che si comportano da entità isolate, i gel non hanno resistenza qualunque sia l'entità della forza da sopportare.
E' possibile comprendere le caratteristiche meccaniche dei gel presumendo che possiedano un grado di reticolazione moderato. Infatti, se i gel non fossero abbastanza elastici, si romperebbero prima di riuscire a misurare alcuni parametri come la resistenza a trazione, l'allungamento e il modulo di elasticità, o mostrebbero una deformazione permanente che renderebbe difficile la valutazione quantitativa delle proprietà meccaniche.
La dipendenza della resistenza dal grado di reticolazione rende ragione del fatto che aumentando la reticolazione aumentano l'elasticità e la resistenza, però non con la stessa progressione; questo significa che, ad esempio, per realizzare un materasso di gel si deve ottenere un grado di reticolazione tale da costituire un compromesso: essere sufficientemente elastico per garantire la comodità e abbastanza resistente da sopportare il peso del corpo.
Un altro parametro tipico dei un polimeri è la temperatura di transizione vetrosa (glass transition temperature). Questo fenomeno, si verifica solo nei polimeri e costituisce una delle caratteristiche che li rendono unici. La temperatura di transizione vetrosa, Tg, è quella temperatura (diversa per ogni polimero) al di sotto della quale un polimero (da morbido e pieghevole) diventa rigido e fragile come il vetro. Alcuni polimeri vengono utilizzati al di sopra delle loro temperature di transizione, altri al di sotto. Le plastiche rigide come il polistirene e il polimetilmetacrilato vengono utilizzate al di sotto delle loro temperature di transizione; ovverosia nel loro stato vetroso. Ciò è possibile in quanto le loro Tg si collocano molto al di sopra della temperatura ambiente, a circa 100°C. Le plastiche flessibili come il polietilene ed il polipropilene sono utilizzate al di sopra della loro Tg, che conferisce loro uno stato gommoso. Gli elastomeri gommosi come poliisoprene e poliisobutilene sono soffici e flessibili cioè quando sono usati al di sopra delle loro Tg. Il polvinilacetato ha Tg = 29 ºC e questo può rappresentare un problema in quanto le proprietà meccaniche del materiale sono fortemente influenzate da variazioni anche limitate della temperatura. Il polivinilacetato è ampiamente utilizzato nell'ambito delle vernici ma anche nel campo delle resine adesive.
 La transizione vetrosa non è una transizione termodinamica (ad es. passaggi di stato), bensì cinetica, in quanto non si hanno cambiamenti nella disposizione spaziale di atomi o molecole (ad es. solidificazione dell'acqua con formazione di una struttura organizzata). In corrispondenza della transizione vetrosa aumenta la mobilità delle catene che costituiscono il polimero, che, comunque, conserva la disorganizzazione strutturale dello stato amorfo.
La transizione vetrosa non è una transizione termodinamica (ad es. passaggi di stato), bensì cinetica, in quanto non si hanno cambiamenti nella disposizione spaziale di atomi o molecole (ad es. solidificazione dell'acqua con formazione di una struttura organizzata). In corrispondenza della transizione vetrosa aumenta la mobilità delle catene che costituiscono il polimero, che, comunque, conserva la disorganizzazione strutturale dello stato amorfo.
tipologie di gel
I gel come quelli menzionati sopra, con un'ottima capacità di assorbire acqua o solventi acquosi (tipicamente fino al 20% del loro peso), vengono chiamati idrogel. Mentre i gel in generale sono ampiamente usati per un numero di diverse applicazioni, l'interesse per gli idrogel sta crescendo costantemente, particolarmente come biomateriali. Dalle lenti a contatto (che permettono un'ottima ossigenazione) ai sistemi trasndermici per il rilascio modificato di farmaci (gel di polisaccaridi sono usati per colntrollare il rilascio di farmaco che, inserito nel reticolo polimerico, viene rilasciato solo quando il sistema è posto a contatto con un solvente esterno).
I sistemi a rilascio modificato (p. e. le pompe osmotiche), per motivi di stabilità, vengono conservati nella stragrande maggioranza dei casi allo stato secco (con l'eccezione di alcuni gel ad uso oftalmico), quindi in assenza della fase liquida rigonfiante. In questo stato, il farmaco in essi contenuto, può trovarsi disperso nel reticolo polimerico secco in forma di microcristalli, nanocristalli o a livello molecolare (questa condizione corrisponde allo stato amorfo) in ragione delle proprietà chimico-fisiche della coppia farmaco-polimero e della tecnica di caricamento del farmaco nel reticolo polimerico (v. fig. 11).
Infatti, lo stato fisico del farmaco nel reticolo polimerico secco è dipende dall'energia fornita per il caricamento, dalle interazioni chimico-fisiche farmaco-polimero e dalla geometria dei cristalli di farmaco che devono collocarsi nelle maglie polimeriche piuttosto serrate a causa dell'assenza della fase liquida. In tali condizioni, il farmaco, per ragioni d'ingombro sterico, non può diffondere nel reticolo verso l'esterno e quindi il sistema si trova in uno stato quiescente e stabile. Non appena viene posto a contatto con un solvente esterno (acqua o liquidi fisiologici), si verifica una serie di fenomeni che danno origine al rilascio del principio attivo: il solvente, penetrando ed allargando le maglie del polimero (micromoto browniano), permette la dissoluzione del principio attivo e quindi il rilascio nell'ambiente esterno. Il rilascio, conseguentemente, dipenderà dalle modalità di diffusione del solvente nel reticolo polimerico, dalla cinetica di dissoluzione del farmaco nel solvente entrante e dalla diffusione del farmaco stesso nella matrice polimerica in via di rigonfiamento. In ultima analisi, la struttura gel regola la cessione del farmaco in base alle proprie caratteristiche di rigonfiamento e di interazione con il farmaco.
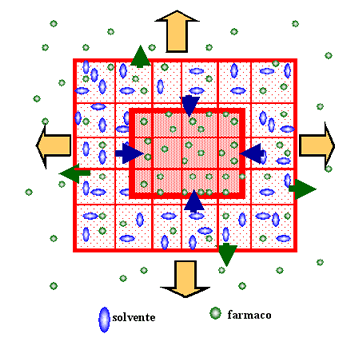 |
| Fig. 11 - Rappresentazione schematica del rilascio di un farmaco da un gel che si rigonfia messo a contatto con un solvente esterno (le catene polimeriche sono schematizzate da linee rosse). Mentre il volume del gel aumenta (frecce gialle), il farmaco è rilasciato (frecce verdi). Durante il rilascio esiste ancora una zona gel non rigonfiata che va via restringendosi (frecce blu) fino a scomparire permettendo il completo rilascio del farmaco.1 |
Le sostanze solubili nel componente liquido si distribuiscono nel gel per diffusione attraverso i micropori e la velocità di diffusione attraverso il gel sarà determinata oltre che dai fattori che determinano la diffusione nelle soluzioni semlici, anche dai fattori legati alla presenza del reticolo. La velocità di diffusione è data dalla legge di Fick:
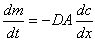
dove: D = coeff. di diffusione, dipende dalla natura dei partecipanti al processo e dalla temperatura [D] = [cm]2 [sec]-1
A = area della sezione interessata al processo diffusivo [A] = [cm]2
 Un fenomeno di rilevante interesse è il cosiddetto "effetto setaccio": gli ioni e le molecole di piccole dimensioni diffondono attraverso i gel con velocità confrontabili con quella che hanno nelle soluzioni. D'altra parte, quando le dimensioni molecolari si avvicinano alla dimensione delle maglie che formano l'intelaiatura reticolare, la diffusione, legata al micromoto browniano, viene ostacolata e cessa del tutto quando le molecole hanno dimensioni superiori a quella delle maglie. Questo fenomeno viene utilizzato per separare composti a diversa dimensione molecolare.
Un fenomeno di rilevante interesse è il cosiddetto "effetto setaccio": gli ioni e le molecole di piccole dimensioni diffondono attraverso i gel con velocità confrontabili con quella che hanno nelle soluzioni. D'altra parte, quando le dimensioni molecolari si avvicinano alla dimensione delle maglie che formano l'intelaiatura reticolare, la diffusione, legata al micromoto browniano, viene ostacolata e cessa del tutto quando le molecole hanno dimensioni superiori a quella delle maglie. Questo fenomeno viene utilizzato per separare composti a diversa dimensione molecolare.
1Mario Grassi - Polisaccaridi: interessanti biopolimeri per usi industriali
(www.enco-journal.com/journal/ej25/grassi.html)
capacità di assorbimento
Un parametro caratteristico del gel è la capacità di aumentare il volume. In senso fisico, la capacità di aumentare il volume dà un'indicazione della quantità di solvente trattenuta dal gel. Matematicamente è una relazione tra il peso (o il volume) occupato dal gel rigonfiato, W(s), e il peso (o volume) occupato dal corrispondente gel asciutto, W(d):
se si considerano i pesi, il rapporto di rigonfiamento all'equilibrio, qw, è dato da:
se vengono considerati i volumi, il rapporto di rigonfiamento all'equilibrio, qv, è dato da:
si può anche definire la percentuale di rigonfiamento, %SD, data da:
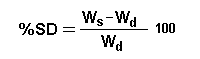
La capacità di aumentare il proprio volume dipende essenzialmente dalla natura del solvente e della catena del polimero, e nei polielettroliti (come i poliacrilici acidi) dipende anche dal grado di dissociazione. Tuttavia, un gel morbido non implica necessariamente che abbia un elevata capacità di aumentare il proprio volume. Molte volte, la scarsa capacità di aumentare il volume è attribuita e catene polimeriche a basso peso molecolare.
La capacità di aumentare il proprio volume ha una rilevante importanza per il gel: più solvente riesce ad assorbire, maggiore è la capacità di aumentare il proprio volume. Alcuni gel come la poliacrilammide, l'alcol polivinilico e l'acido poliacrilico sono superassorbenti: possono trattenere una quantità enorme di acqua. Per esmpio,
l'imbottitura dei pannolini è costituita da acido poliacrilico che può assorbire una quantità di acqua nettamente superiore al suo peso, permettendo all'infante di rimanere asciutto e pulito.
Il vantaggio di avere pannolini con acido poliacrilico all'interno, a parte il fatto di essere meno impregnati, è che una volta bloccata tutta l'urina all'interno dell'acido poliacrilico, l'infante rimane asciutto senza avere problemi di arrossamento della pelle.
gel "intelligenti"
Come abbiamo riassunto, i campi di applicazione dei gel sono sempre più vasti, specialmente con la disponibilità dei cosiddetti "gel intelligenti". Intelligenti (sebbene passivamente) perché il loro aumento di volume può essere collegato a cambiamenti legati a fattori ambientali come temperatura, pH, solventi, forza ionica, intensità della luce, pressione, onde ultrasoniche e campi elettrici e magnetici. Variando la temperatura di solo 1°C, è possibile provocare un aumento di volume del gel di centinaia di volte il suo peso, o farlo collassare, o persino quando non aumenta di volume, si può notare la sua capacità di cambiare le sue proprietà fisiche.
Sin dalla loro scoperta nel 1975, i gel intelligenti sono stati testati in un numero di
prodotti differenti. Le suole delle scarpe in gel sono così comode perché sono usati gel viscoelastici che sono morbidi alla temperatura ambiente, ma diventano duri quando entrano in contatto con il corpo umano, reagendo al variare della temperatura.
La proprietà di cambiare le loro proprietà e l'aderenza al tessuto biologico, è un'altra caratteristica mostrata dagli idrogel come l'acido poliacrilico: con l'aggiunta di qualche farmaco nella matrice del gel, si ottengono prodotti utili per le applicazioni farmaceutiche come gocce per gli occhi o per il naso o creme per il sole. Questo perché il gel diventa più viscoso quando raggiunge gli occhi e il naso, prevenendo le gocce dalla diluizione come nel caso di gocce per gli occhi.  Una volta collocato nel sito d'azione, il gel ha la capacità rilasciare il farmaco per un lungo periodo di tempo.
Una volta collocato nel sito d'azione, il gel ha la capacità rilasciare il farmaco per un lungo periodo di tempo.
Con le creme solari, il comportamento è differente. Le creme solari tradizionali sono solitamente unte, così vengono assorbite dalla pelle raggiungendo il flusso del sangue, dove la loro utilità è nulla. Al contrario, gli idrogel sono acquosi; intrappolano al loro interno gli agenti bioattivi e rimangono sulla pelle molto più a lungo.
gel corporei
I nostri muscoli e gli organi interni sono degli idrogel. In effetti il nostro corpo è costituito anche da proteine (polimeri naturali), circondate da enormi quantità dacqua. Dopo tutto, circa 80%del corpo degli animali è costituito dacqua!
Se mettiamo queste proteine in contatto con l'acqua, si ottiene una voluminoso idrogel. Tutte le parti soffici del nostro corpo sono soltanto un grosso gel, dove si ha un continuo cambiamento nella dimensione molecolare e del grado di reticolazione.
Gli idrogel giocano un ruolo chiave nelle nuove scoperte di biotecnologia, il gel chimico non è solo circoscritto alla molecole organiche. Infatti ci sono molti gel inorganici, ovviamente derivati da polimeri inorganici, in particolare il silicone e i polisilani. C'è un altro importante ramo del gel chimico, chiamato sol-gel chimico che è applicato nel campo del vetro e delle ceramiche, dove la ricerca è ancora intensa.
Comunemente il processo del sol-gel consiste nella preparazione di una rete polimerica,
lavorando in una soluzione a basse temperature. La reazione evolve in tre principali fasi: la formazione di una sospensione colloidale, (chiamata "sol") il seguente raffreddamento del sol in una fase liquida continua ("gel") e la rimozione del solvente.
Marcello Guidotti
adattato, modificato e rielaborato da:
Department of Polymer
Science | University of Southern Mississippi
 1 1 |
 2 2 |
 3 3 |
 4 4 |
 5 5 |
 6 6 |
 7 7 |
 8 8 |
9 |
 HOME PAGE HOME PAGE |
 Ad esempio, l'acido solfidrico ha una struttura simile a quella dell'acqua ed ha un peso molecolare maggiore dell'acqua (32 contro 18), eppure a temperatura ambiente l'acido solfidrico è un gas e l'acqua è in fase liquida. Questo perché l'acqua è molto polare, tanto da formare legami idrogeno intermolecolari che permettono alle molecole di rimanere in fase liquida; al contrario, l'acido solfidrico non è sufficientemente polare da permettere alle sue molecole di attrarsi reciprocamente.
Ad esempio, l'acido solfidrico ha una struttura simile a quella dell'acqua ed ha un peso molecolare maggiore dell'acqua (32 contro 18), eppure a temperatura ambiente l'acido solfidrico è un gas e l'acqua è in fase liquida. Questo perché l'acqua è molto polare, tanto da formare legami idrogeno intermolecolari che permettono alle molecole di rimanere in fase liquida; al contrario, l'acido solfidrico non è sufficientemente polare da permettere alle sue molecole di attrarsi reciprocamente.










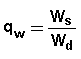
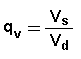
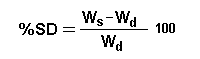
 Una volta collocato nel sito d'azione, il gel ha la capacità rilasciare il farmaco per un lungo periodo di tempo.
Una volta collocato nel sito d'azione, il gel ha la capacità rilasciare il farmaco per un lungo periodo di tempo.