caratteristiche e proprietà delle emulsioni
Le emulsioni sono sistemi dispersi, cioè eterogenei, costituiti da due fasi liquide immiscibili tra loro. Possiamo distinguere emulsioni di olio in acqua (O/A, Oil/Water) ed emulsioni di acqua in olio (A/O, W/O). Nel primo tipo l'olio rappresenta la fase dispersa (o discontinua o interna) e l'acqua la fase disperdente (o continua o esterna); il contrario avviene per le emulsioni A/O. Per es., il latte ed il burro sono due emulsioni naturali, rispettivamente O/A e A/O.
emulsioni
Per stabilire il tipo di emulsione in esame, si può ricorrere a vari metodi:
- diluizione: se una data emulsione è diluibile in acqua (ad es., latte, maionese) è di tipo O/A; nel caso contrario è di tipo A/O (ad es., burro, margarina);
- uso di coloranti: un'emulsione addizionata con un colorante idrosolubile (ad es., blu di metilene), risulterà uniformemente colorata se è di tipo O/A. Se il colorante aggiunto all'emulsione è liposolubile (ad es., sudan - non per uso alimentare), si avrà colorazione uniforme se l'emulsione è di tipo A/O;
- conducibilità elettrica: poiché l'olio, al contrario dell'acqua conduce la corrente elettrica in misura estermamente ridotta, è ovvio che solo le emulsioni di tipo O/A permetteranno il passaggio di corrente fra due elettrodi;
- fluorescenza: la maggior parte deglio olii, e quindi le emulsioni A/O, emettono fluorescenza se eccitati con radiazioni elettromagnetiche di opportuna lunghezza d'onda.
Dal punto di vista farmaceutico, vengono utilizzate molte emulsioni (A/O e O/A) per uso topico, mentre è meno diffuso l'uso di emulsioni per uso orale (O/A); esistono infine anche particolari emulsioni multiple, ad es. O/A/O. Le dimensioni delle goccioline nella fase dispersa variano da 0.1 a 0.5 mm, ma esistono anche microemulsioni in cui le dimensioni scendono sotto il limite inferiore e ciò conferisce loro un aspetto trasparente in quanto non costituiscono più un ostacolo alla propagazione rettilinea delle luce (v. colloidi).
 |
|
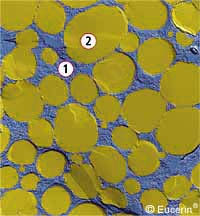 |
| immagine al microscopio elettronico di una emulsione O/A : 1) fase acquosa esterna; 2) fase oleosa interna (tratta dal sito: www.eucerin.co.uk)
|
|
immagine al microscopio elettronico di una emulsione O/A con maggior contenuto di olio: 1) fase acquosa esterna; 2) fase oleosa interna (tratta dal sito: www.eucerin.co.uk) |
Un problema fondamentale consiste nel prevedere il tipo di emulsione che si formerà dalla agitazione di due fasi immiscibili, e ciò dipende da vari fattori:
- volume di fase: è il rapporto tra la percentuale della fase acquosa e quello della fase oleosa. L'entità di questo fattore è legata alla tendenza delle goccioline, che costituiranno o dovranno costituire la fase dispersa, a coalescere, ovverosia a riunirsi tra loro per ricostituire una fase continua. In particolare, poiché la coalescenza aumenta in misura proporzionale al numero di goccioline disperse, la fase presente in quantità maggiore avrà maggior tendenza a costituire la fase continua. D'altra parte, con opportuni tensioattivi e per determinati valori di viscosità, si può limitare fino al 10% la percentuale di fase continua nell'emulsione; tuttavia, queste emulsioni sono poco stabili in quanto la fase presente in quantità maggiore avrà sempre la tendenza a divenire la fase continua, con inversione dell'emulsione ad es. da O/A a A/O.
In pratica, è comunque raro che si preparino emulsioni in cui la fase continua sia percentualmente minore della fase discontinua, così, al massimo, in alcuni cosmetici si arriva ad un 60% di fase continua.
- viscosità delle fasi: la fase più viscosa si suddividerà meno facilmente producendo un minor numero di goccioline e quindi avrà maggior tendenza a costituire la fase continua.
- tensioattivi: l'azione emulsionante di un tensioattivo si può spiegare facilmente pensando che costituisce una sorta di "ancoraggio" tra le gocciolone che costituiscono la fase discontinua ed il liquido che costituisce la fase continua. Per prevedere l'azione prodotta da un tensioattivo sulla dispersione di due liquidi immiscibili, si ricorre alla regola di Bancroft: la fase continua è quella in cui il tensioattivo è più solubile.
 La regola di Bancroft, trova il suo fondamento teorico ove si consideri che l'abbassamento della tensione superficiale di un liquido ne favorisce la frammentazione in gocce; sicché, se mescoliamo due liquidi immiscibili tra loro addizionandovi un tensioattivo, questo ridurrà in misura minore la tensione superficiale del liquido in cui è più solubile (la riduzione della tensione avviene alla superficie di un liquido) e sarà quindi questo liquido che si comporterà da fase esterna.
La regola di Bancroft, trova il suo fondamento teorico ove si consideri che l'abbassamento della tensione superficiale di un liquido ne favorisce la frammentazione in gocce; sicché, se mescoliamo due liquidi immiscibili tra loro addizionandovi un tensioattivo, questo ridurrà in misura minore la tensione superficiale del liquido in cui è più solubile (la riduzione della tensione avviene alla superficie di un liquido) e sarà quindi questo liquido che si comporterà da fase esterna.
Così, ad es., poiché la solubilità in acqua di un tensioattivo aumenta con il valore di HLB, è logico che tensioattivi con elevato HLB diano prevalentemente emulsioni O/A.
Il fenomeno della coalescenza, fà sì che qualsiasi emulsione sia soggetta a destabilizzarsi; in questo processo possiamo distinguere tre stadi:
- flocculazione: le goccioline della fase discontinua iniziano a coalescere (questo stadio è reversibile);
- scrematura: il flocculato sale in superficie (stadio reversibile, ma più difficile da trattare);
- separazione delle fasi: l'emulsione si "rompe" definitivamente ed irreversibilmente.
 Anche l'accennata inversione dell'emulsione può ritenersi, se indesiderata, destabilizzante: in particolare, questa può verificarsi o quando il volume della fase discontinua è troppo elevato o per azione di un tensioattivo. Ad es., se si impiega come tensioattivo un sapone sodico (idrosolubile) e nella fase continua sono presenti ioni calcio, questi trasformeranno il sapone in calcico (liposolubile) e ciò può favorire l'inversione.
Anche l'accennata inversione dell'emulsione può ritenersi, se indesiderata, destabilizzante: in particolare, questa può verificarsi o quando il volume della fase discontinua è troppo elevato o per azione di un tensioattivo. Ad es., se si impiega come tensioattivo un sapone sodico (idrosolubile) e nella fase continua sono presenti ioni calcio, questi trasformeranno il sapone in calcico (liposolubile) e ciò può favorire l'inversione.
stabilità delle emulsioni
Abbiamo discusso come individuare il tipo di emulsione in esame, come prevedere il tipo di emulsione che si formerà ed i suoi stadi destabilizzanti. Ora esamineremo i fattori che concorrono a stabilizzare le emulsioni.
- agente emulsionante: generalmente è un tensioattivo, che abbassando la tensione interfacciale diminuisce l'energia libera del sistema; in alternativa, si possono utilizzare anche sostanze non tensioattive, quali la gomma arabica, la gelatina, colloidi idrofili o polveri finemente suddivise (ad es., talco). Queste sostanze si distribuiscono all'interfase O/A formando una pellicola protettiva, più rigida di quella formata dai tensioattivi, che costituisce una barriera verso la coalescenza. Per contro, sostanze con forte affinità per l'acqua (come gli zuccheri) possono sottrarre acqua alle interfasi rompendo l'emulsione.
- barriera all'interfase: la superficie definita dall'incontro tra la fase continua e le goccioline che costituiscono la fase discontinua, è elettrostaticamente carica indipendentemente dalla natura ionica o non ionica del tensioattivo. Infatti, la carica sempre presente sulla barriera è dovuta o alla natura polare di una delle due fasi, o agli attriti (che generano una carica elettrostatica), o ancóra all'adsorbimento di ioni presenti in soluzione (anche i tensioattivi si dispongono all'interfase per adsorbimento). E' quindi evidente che le sostanze ionizzabili (come i sali) possono interferire con le cariche superficiali diminuendo le forze repulsive e facilitando la coalescenza.
- viscosità del mezzo, velocità di sedimentazione o scrematura, dimensione delle particelle: questi fattori sono correlati tra loro dalla legge di Stokes. Da questa legge si deduce che il sistema sarà tanto più stabile quanto più le densità delle due fasi sono vicine e quanto maggiore è la viscosità della fase continua; inoltre, si cercherà di ridurre quanto più possibile le dimensioni delle particelle, ottimizzandone le dimensioni (con successive prove sperimentali) in funzione del tensioattivo impiegato che ne controlla la stabilità.
scelta del tensioattivo
Per poter scegliere il tensioattivo più efficace, viene fatto corrispondere (v. tabella) alle più comuni fasi oleose, il cosiddetto HLBr (r = richiesto) del tensioattivo più adatto per formare l'emulsione più stabile.
| sostanza |
HLBr O/A |
sostanza |
HLBr O/A |
| acido laurico |
16 |
olio di oliva |
7 |
| acido linoleico |
16 |
olio di ricino |
14 |
| acido oleico |
17 |
olio di sesamo |
7 |
| acido stearico |
17 |
olio di semi di carote |
6 |
| alcol cetilico |
15 |
olio di semi di cotone |
7,5 |
| burro di cacao |
6 |
olio di semi di girasole |
7 |
| cera carnauba |
12 |
olio di soia |
7 |
| cera d'api |
9 |
olio di vaselina |
10 |
| lanolina |
12 |
paraffina |
10 |
| olio di avocado |
7 |
olio di semi di mango |
7 |
| olio di cocco |
8 |
olio di semi di borragine |
7 |
| olio di Jojoba |
6,5 |
olio di arachidi |
6 |
Per determinare l'HLBr di un'emulsione, si preparano una decina di emulsioni stabilizzate da tensioattivi con HLB differenti, assegnando l'etichetta HLBr all'emulsione più stabile. Il valore dell'HLBr sarà ovviamente diverso a seconda che l'olio costituisca la fase continua o la fase discontinua. Noto il valore di HLBr, si può scegliere il tensioattivo più adatto, non solo come indice di HLB, ma anche in base a compatibilità chimiche e norme legislative. A tale scopo, è generalmente conveniente miscelare due tensioattivi, calcolando la loro presenza percentuale in miscela graficamente o analiticamente.
L'indice HLB è una grandezza estensiva (i suoi valori possono essere sommati algebricamente) e quindi è possibile prevedere gli effetti della combinazione risultante dall'associazione di due tensioattivi semplicemente calcolando la media aritmetica dei corrispondenti indici. Ad es., mescolando in parti uguali uno Span con HLB = 3 ed un Tween con HLB = 15, avremo una miscela con HLB = (3 + 15)/2 = 9. Questo fatto è molto utile in quanto per preparare certe emulsioni, sono richiesti dei particolari valori di HLBr che sono facilmente ottenibili miscelando due tensioattivi.
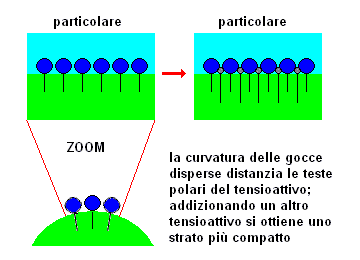 E' possibile giustificare intuitivamente l'effetto della combinazione di due tensioattivi: si osservi la figura a destra, dove sono schematizzati due tipi di tensioattivi con affinità per le fasi acquosa ed oleosa leggermente diversa. Risulta evidente la possibilità che i due tensioattivi si inseriscano nella fase acquosa in modo da formare uno strato più compatto.
E' possibile giustificare intuitivamente l'effetto della combinazione di due tensioattivi: si osservi la figura a destra, dove sono schematizzati due tipi di tensioattivi con affinità per le fasi acquosa ed oleosa leggermente diversa. Risulta evidente la possibilità che i due tensioattivi si inseriscano nella fase acquosa in modo da formare uno strato più compatto.
In generale, nella miscelazione di due tensioattivi, l'ottenimento di un particolare valore di HLB
comporta che le concentrazioni dei due singoli tensioattivi siano diverse ed è possibile valutarle sia analiticamente che graficamente. Supponiamo, per es., di voler determinare le percentuali, x ed y, di due tensioattivi caratterizzati rispettivamente dai valori HLBx ed HLBy, necessarie per ottenere una miscela con indice HLBr.
Posto x + y = 1 (ossia la somma delle percentuali secondo cui vengono miscelati i due tensioattivi), risulta:
HLBr = (x) (HLBx) + (1 - x) (HLBy)
risolvendo rispetto ad x, ed esprimendo il risultato come percentuale, si ottiene:
esempio: per concretizzare quanto discusso, si consideri la preparazione cosmetica riportata a destra, che essendo costituita da più componenti, richiede un calcolo a parte per l'HLBr:
| olio di vaselina |
33 parti |
| lanolina |
2 parti |
| alcol cetilico |
1 parte |
| emulsionante |
5 parti |
| acqua |
q.b. a 100 |
Le singole percentuali dei componenti (escluso l'emulsionante), sono:
olio di vaselina = (33/36) · 100 = 91.66%
lanolina = (2/36) · 100 = 6.05%
alcol cetilico = (1/36) · 100 = 2.77%
poiché i rispettivi HLB riferiti alle sostanze singole sono: 10, 12, 15 (cfr. tabella precedente), il valore di HLBr richiesto per preparare l'emulsione più stabile con la loro associazione, sarà:
HLBr = (10 · 91.66 + 12 · 6.05 + 15 · 2.77 )/100 = 10.24
Per completare la preparazione, rimane da addizionare l'emulsionante (5 parti): per ottenere l'HLBr = 10.24 , si può miscelare uno Span con HLB = 3 e un Tween con HLB = 15
10.24 = x (15) + (1 - x) (3) da cui si ricava per il Tween x = 0.6
i due tensioattivi devono essere combinati nelle percentuali Tween 60% e Span 40% , che per 5 parti di emulsionante corrispondono a 3 parti di Tween e 2 parti di Span.
Il procedimento analitico può essere efficacemente sostituito utilizzando grafici già predisposti (come quello riportato in figura a destra), dove in ordinate sono riportati, da ambo il lati, i valori di HLB corrispondenti a vari tensioattivi, ed in ascissa una doppia scala fornisce i valori relativi delle concentrazioni espresse in percentuale. Il principio del metodo è basato sulla dipendenza della combinazione lineare dell'HLB dalle concentrazione.
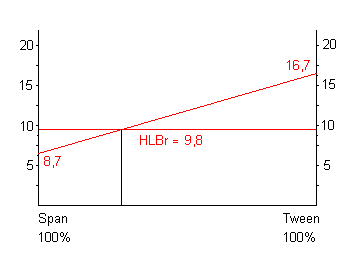 Supponiamo, ad es., di voler realizzare una miscela di tensioattivi per preparare un'emulsione il cui HLBr = 9.8, avendo a disposizione uno Span 40 (HLB = 6.7) ed un Tween 20 (HLBr = 16.7). La miscelazione produce, in corrispondenza delle loro relative concentrazioni, una serie di valori HLB, riportati su una retta da 8.7 a 16.7, sicché la composizione percentuale della miscela avente HLBr si ottiene dall'intersezione di questa retta con la retta parallela all'asse delle sacisse e passante per il valore HLBr = 9.8
Supponiamo, ad es., di voler realizzare una miscela di tensioattivi per preparare un'emulsione il cui HLBr = 9.8, avendo a disposizione uno Span 40 (HLB = 6.7) ed un Tween 20 (HLBr = 16.7). La miscelazione produce, in corrispondenza delle loro relative concentrazioni, una serie di valori HLB, riportati su una retta da 8.7 a 16.7, sicché la composizione percentuale della miscela avente HLBr si ottiene dall'intersezione di questa retta con la retta parallela all'asse delle sacisse e passante per il valore HLBr = 9.8
Il calcolo numerico può essere impiegato per la determinazione dell'HLB di un tensioattivo. Si procede in questo modo: si preparano alcune miscele, in varie proporzioni, di un tensioattivo avente HLBn (n = noto) con il tensioattivo di cui non si conosce l'HLBi (i = incognito). Poi, con queste miscele, si prepara una emulsione di cui si conosca l'HLBr. Alla miscela di tensioattivi che dà l'emulsione più stabile, si assegna il valore di HLBr e quindi si calcola l'HLBi con questo procedimento:
posto x + y = 1 (ossia la somma delle percentuali secondo cui vengono miscelati i due tensioattivi), risulta:
(x) HLBi + (1 - x) HLBn = HLBr
essendo noti HLBn ed HLBr, risolvendo questa equazione, si ricava HLBi
due classiche emulsioni galeniche
L'emulsione riportata nella ricetta in basso a sinistra, è una classica emulsione lassativa, la cui azione deriva dalla presenza dell'olio di vaselina. In questo caso, per mascherarne il sapore, si formula un'emulsione O/A edulcorata con saccarosio.
La stabilizzazione di questa emulsione, che si presenta come una forma sciropposa piuttosto viscosa, non è affidata alla presenza di tensioattivi, bensì alle gomme, che ne aumentano la viscosità ostacolando la separazione delle fasi.
L'emulsione riportata nella ricetta in basso a destra, è la cosiddetta cold cream. In questo caso, per conferire caratteristiche più adatte all'uso topico, si formula un'emulsione A/O .
La stabilizzazione di questa emulsione, che si presenta come una forma cremosa, è affidata alla presenza di un tensioattivo prodotto in situ dalla salificazione dell'acido cerotico - contenuto nella cera - con l'acido borico.
Le due preparazioni citate sono riportate nella loro formulazione classica e quindi il tipo e la quantità di tensioattivo non deve essere calcolata (come è stato fatto negli esempi proposti): è un pò come la pasta alla carbonara, si può modificarne la ricetta (come faccio io perché sono vegetariano) ma allora non è più pasta alla carbonara... è un'altra cosa.
| olio di vaselina |
g 22,50 |
| gomma arabica |
g 6,25 |
| gomma adragante |
g 0,40 |
| saccarosio |
g 4,00 |
| acqua depurata |
q.b. a g 50,00 |
| cera bianca |
g 3,00 |
| spermaceti |
g 3,50 |
| olio di vaselina |
g 17,00 |
| sodio borato |
g 0,20 |
| acqua depurata |
g 6,00 |
|
 1 1 |
 2 2 |
 3 3 |
4 |
 5 5 |
 6 6 |
 7 7 |
 8 8 |
 9 9 |
 10 10 |
 11 11 |
 12 12 |
 13 13 |
 14 14 |
 15 15 |
 HOME PAGE HOME PAGE |
Marcello Guidotti, copyright 2003-2004-2005-2006-2009
questa pagina può essere riprodotta su qualsiasi supporto o rivista purché sia citata la fonte e l'indirizzo di questo sito (ai sensi degli artt. 2575 e 2576 cc. Legislazione sul diritto d'autore). Le fotografie sono tratte da siti web e sono, o possono ritenersi, di pubblico dominio purché utilizzate senza fini di lucro. Le immagini di prodotti presenti nel sito hanno unicamente valenza esemplificativa oltre che, eventualmente, illustrare messaggi fuorvianti e non vi è alcun richiamo diretto o indiretto alla loro qualità e/o efficacia il cui controllo è affidato alle autorità regolamentatorie.


 La regola di Bancroft, trova il suo fondamento teorico ove si consideri che l'abbassamento della tensione superficiale di un liquido ne favorisce la frammentazione in gocce; sicché, se mescoliamo due liquidi immiscibili tra loro addizionandovi un tensioattivo, questo ridurrà in misura minore la tensione superficiale del liquido in cui è più solubile (la riduzione della tensione avviene alla superficie di un liquido) e sarà quindi questo liquido che si comporterà da fase esterna.
La regola di Bancroft, trova il suo fondamento teorico ove si consideri che l'abbassamento della tensione superficiale di un liquido ne favorisce la frammentazione in gocce; sicché, se mescoliamo due liquidi immiscibili tra loro addizionandovi un tensioattivo, questo ridurrà in misura minore la tensione superficiale del liquido in cui è più solubile (la riduzione della tensione avviene alla superficie di un liquido) e sarà quindi questo liquido che si comporterà da fase esterna. E' possibile giustificare intuitivamente l'effetto della combinazione di due tensioattivi: si osservi la figura a destra, dove sono schematizzati due tipi di tensioattivi con affinità per le fasi acquosa ed oleosa leggermente diversa. Risulta evidente la possibilità che i due tensioattivi si inseriscano nella fase acquosa in modo da formare uno strato più compatto.
E' possibile giustificare intuitivamente l'effetto della combinazione di due tensioattivi: si osservi la figura a destra, dove sono schematizzati due tipi di tensioattivi con affinità per le fasi acquosa ed oleosa leggermente diversa. Risulta evidente la possibilità che i due tensioattivi si inseriscano nella fase acquosa in modo da formare uno strato più compatto. 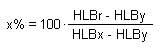
 Supponiamo, ad es., di voler realizzare una miscela di tensioattivi per preparare un'emulsione il cui HLBr = 9.8, avendo a disposizione uno Span 40 (HLB = 6.7) ed un Tween 20 (HLBr = 16.7). La miscelazione produce, in corrispondenza delle loro relative concentrazioni, una serie di valori HLB, riportati su una retta da 8.7 a 16.7, sicché la composizione percentuale della miscela avente HLBr si ottiene dall'intersezione di questa retta con la retta parallela all'asse delle sacisse e passante per il valore HLBr = 9.8
Supponiamo, ad es., di voler realizzare una miscela di tensioattivi per preparare un'emulsione il cui HLBr = 9.8, avendo a disposizione uno Span 40 (HLB = 6.7) ed un Tween 20 (HLBr = 16.7). La miscelazione produce, in corrispondenza delle loro relative concentrazioni, una serie di valori HLB, riportati su una retta da 8.7 a 16.7, sicché la composizione percentuale della miscela avente HLBr si ottiene dall'intersezione di questa retta con la retta parallela all'asse delle sacisse e passante per il valore HLBr = 9.8