|
This text will be replaced
|
Il video a destra mostra la diffusione di un colorante alimentare in acqua. Il fatto sembra banale; tuttavia, se si osserva attentamente la diffusione del colorante, si vede che il liquido non si disperde liberando le sue molecole in tutte le direzioni, bensì forma una sorta di cordoncino che si sfilaccia, si ripiega su se stesso e lentamente, molto lentamente diffonde nell'acqua.
Dopo aver visto questo video, ci proponiamo di comprendere il curioso comportamento di questo processo diffusivo che verosimilmente ci è capitato di vedere molte volte, però prestandovi poca attenzione proprio perché molto comune.

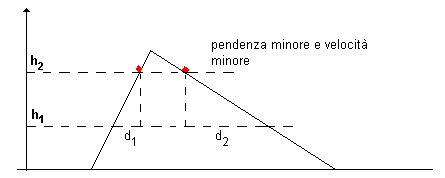
Si considerino due cubetti posti su un doppio piano inclinato privo di attrito. La velocità con cui diminuisce la quota dei due cubetti allorché prendono a scivolare lungo i due piani, dipenderà dall'inclinazione di questi ultimi in quanto determinerà una maggior o minore velocità di scivolamento. In particolare, a parità di altezza, se i due cubetti sono lasciati scivolare contemporaneamente dai versanti opposti, quello che segue il percorso più ripido raggiungerà il piano per prima (si noti tuttavia, che la velocità massima raggiunta al piano è uguale per entrambi i percorsi in quanto dipende dalla sola altezza: ![]() )
)
In prima approssimazione, possiamo concludere che la velocità di ogni cubetto è direttamente proporzionale alla pendenza del piano su cui scivolano: cioè direttamente proporzionale al dislivello (h2 - h1) ed inversamente proporzionale alla distanza orizzontale, d, che separa le due quote.
In particolare, a parità di dislivello, il percorso lungo il quale la variazione di quota per unità di distanza orizzontale è massima, prende il nome di gradiente, e quando sono possibili più percorsi, quello più breve è appunto definito dal gradiente.
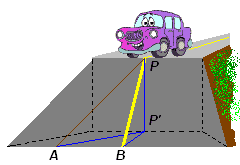
Dopo aver esaminato il caso del profilo monodimensionale (il doppio piano inclinato), vediamo cosa accade in un caso tridimensionale.
 |
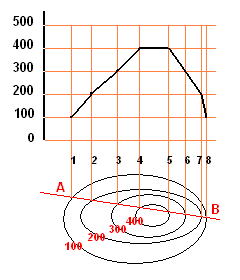 La figura a destra, mostra il profilo longitudinale di un terreno costruito a partire da una serie di curve di livello. Le curve, dette isoipse (stessa quota) sono rappresentate con delle linee chiuse ciascuna delle quali ha associata una quota espressa in metri. Così, procedendo dall'esterno verso l'interno, la prima curva ha una quota di 100 m; la seconda, di 200 m; la terza di 300 m; la quarta di 400 m. Ogni quota differisce dalla precedente per uno stesso valore, in questo caso 100 m.
La figura a destra, mostra il profilo longitudinale di un terreno costruito a partire da una serie di curve di livello. Le curve, dette isoipse (stessa quota) sono rappresentate con delle linee chiuse ciascuna delle quali ha associata una quota espressa in metri. Così, procedendo dall'esterno verso l'interno, la prima curva ha una quota di 100 m; la seconda, di 200 m; la terza di 300 m; la quarta di 400 m. Ogni quota differisce dalla precedente per uno stesso valore, in questo caso 100 m.
Osservando con attenzione le isoipse, si vede che la loro reciproca distanza non è costante: quando le isoipse si avvicinano la loro distanza è minore e così la loro differenza di quota corrisponde ad una pendenza maggiore. Fra tutte le pendenze possibili, quella più ripida è il gradiente. Nella figura, i punti 5 e 8 sono a distanza complessivamente minore rispetto a quelli fra 4 e 1 ed infatti, il profilo lungo AB mostra come da 400 a 100 m, il versante destro della collina sia il più ripido (il risultato può cambiare scegliendo una sezione differente).
Ciò premesso, se lasciamo cadere due sferette lungo il versante sinistro e quello destro (che presenta un gradiente maggiore), la sferetta che scivola lungo quest'ultimo versante raggiungerà il suolo prima dell'altra.
Se ripetiamo lo stesso procedimento utilizzato per tracciare un profilo longitudinale corrispondente all'intercetta con AB con altre intercette è intuitivo che otterremo un'approssimazione tridimensionale di una collina. Da quanto esposto dovrebbe essere chiaro che se lasciamo cadere un certo numero di sferette dalla sommità della collina, queste non raggiungeranno il suolo contemporaneamente, ma ognuna accelererà seguendo il gradiente che definisce la sua traiettoria.
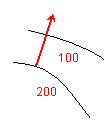
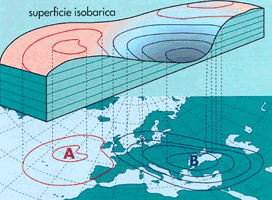 Così come la velocità max di discesa da una collina si ha lungo il percorso di massima pendenza, nella proiezione orizzontale dei dislivelli (cioè sul piano), la velocità max è perpendicolare alle due isoipse (la perpendicolare tra due isoipse, Fig. a sinistra, definisce il gradiente).
Così come la velocità max di discesa da una collina si ha lungo il percorso di massima pendenza, nella proiezione orizzontale dei dislivelli (cioè sul piano), la velocità max è perpendicolare alle due isoipse (la perpendicolare tra due isoipse, Fig. a sinistra, definisce il gradiente).
Seguendo il criterio discusso, se sostituiamo le quote con temperature otteniamo delle curve isoterme (lungo le quali la temperaturà è costante) ed in questo caso il gradiente termico collegherà due punti a differenti temperature la cui distanza è minima. Analogamente, se sostituiamo le quote con pressioni, otteniamo delle curve isobare (indispensabili per le previsioni atmosferiche) ove il gradiente termico collegherà due punti a differenti pressioni la cui distanza è minima.
 La comprensione del concetto di gradiente è essenziale in quanto chiarisce che quando si parla di flussi attraverso lo spazio, occorre pensarli non come se si spostassero su una superficie bidimensionale, ma tridimensionale.
La comprensione del concetto di gradiente è essenziale in quanto chiarisce che quando si parla di flussi attraverso lo spazio, occorre pensarli non come se si spostassero su una superficie bidimensionale, ma tridimensionale.
Per esempio, quando una compressa si dissolve nei fluidi gastrici, il flusso che vi si diffonde è costituito da molecole che si allontanano reciprocamente seguendo i diversi gradienti di concentrazione.
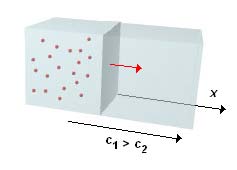 Il flusso molecolare, nella direzione x, ha un verso per cui la concentrazione diminuisce |
Per esprimere quanto discusso in termini analitici, consideriamo il processo di diffusione assumendo quale riferimento un asse x puntato verso destra, cioè nel verso in cui diminuisce la concentrazione.
A rigore, durante il processo diffusivo, la differenza di concentrazione lungo il percorso può variare anche notevolmente. Però, quando si calcola il flusso di diffusione dm/dt fra due regioni a differenti concentrazioni, c1 e c2 (c1 > c2), possiamo ammettere che il flusso in una sezione molto sottile avvenga in una regione a concentrazione costante, c. Pertanto, possiamo scrivere:
![]()
dove:
D = coefficiente di diffusione, dipende dalla natura dei partecipanti al processo e dalla temperatura [D] = [cm]2 [sec]-1
A = area della sezione interessata al processo diffusivo [A] = [cm]2
legge di Fick: il flusso molecolare in ogni punto è proporzionale alla variazione di concentrazione per unità di percorso nella direzione in cui tale variazione è massima ed ha verso opposto a quello in cui diminuiscono le concentrazioni.
Il segno negativo si giustifica in quanto le molecole si spostano nel verso in cui diminuiscono le concentrazioni, e poiché dc/dx risulterebbe negativo, per ottenere un flusso positivo (nella direzione delle x crescenti) è necessario anteporre alla formula il segno negativo.
In particolare, nel caso della diffusione tra due zone a concentrazione diversa, la formula vista, per integrazione, assume la forma:
questa equazione è corretta solo quando le differenze di concentrazione variano in misura costante (C3 - C2 = C2 - C1) e mostra che il flusso molecolare, J, è positivo se (C1 > C2), ossia le concentrazione diminuiscono nel verso in cui aumenta x.
 |
 le molecole di soluto nella soluzione di sinistra (conc. maggiore), diffondono attraverso la membrana in modo da aumentare la conc. nella soluzione di destra. |
Supponiamo che la diffusività D non vari con la concentrazione; allora, come nel caso stazionario, tra due piani distanti Δ x c'è una differenza di concentrazione C2 - C1 e tale concentrazione varia linearmente in funzione della coordinata spaziale x; per conseguenza si produrrà un flusso di materia tra i due piani che tende ad eguagliare le concentrazioni. In condizioni non stazionarie, inoltre, l'intensità del flusso di materia diminuirà al passare del tempo, fino a quando si raggiungerà, in ogni punto, la concentrazione di equilibrio Ce.
Dato un volumetto di spessore dx, la variazione della concentrazione di fluido nel tempo t, è evidentemente legata al flusso, J, di materia che attraversa lo spessore di quel volumetto.
sostituendo la prima legge di Fick si ottiene:
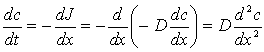 |
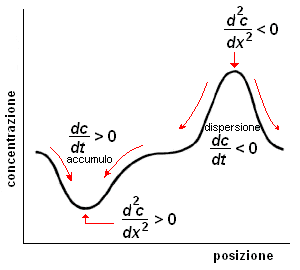
Questa equazione, nota come seconda legge di Fick, sebbene di significato meno evidente, esprime matematicamente un risultato intuitivamente prevedibile: la velocità con la quale le particelle abbandonano una data regione è proporzionale alla disomogeneità spaziale della concentrazione in quella regione rispetto alle zone circostanti (Fig. a destra). Nelle zone in cui le molecole sono presenti in numero maggiore della media (punti di massimo relativo d2c/d x2 < 0) le particelle tendono a disperdersi (segno negativo in quanto il flusso è in verso opposto all'aumento delle concentrazioni) riducendo localmente la concentrazione (dc/dt < 0). Al contrario, se localmente si presenta un minimo della concentrazione (d2c/d x2 > 0), le particelle tenderanno ad accumularvisi (dc/dt > 0).
Come per la prima legge di Fick, anche la seconda può essere integrata ottenendo i valori delle concentrazioni in funzione del tempo. Tuttavia, l'integrazione non è sempre possibile e, particolarmente nel caso dei processi biologici, ha essenzialmente valore indicativo e per la variabilità individuale e perché il coefficiente di diffusione può addirittura variare con la concentrazione. Per questa ragione, in generale, l'orientamento nell'allestimento delle formulazioni farmaceutiche è basato su modifiche della prima legge di Fick.
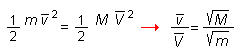
Questo significa che le molecole di un gas si allontanano l'una dall'altra, in tutte le direzioni, ad una velocità molto elevata (nel vuoto l'ordine di grandezza è metri al secondo); in particolare, se si tratta di una miscela gassosa, per esempio monossido di carbonio e biossido di carbonio, le molecole del gas più leggero (CO) si disperderanno mediamente con una velocità maggiore.
La legge di Graham, grazie alle moderne tecniche di analisi ad alta sensibilità, offre un metodo di rilevante interesse per individuare le differenze fra processi naturali e manipolazioni tecnologiche. Per questo, si ricorre al fatto che il carbonio è presente in natura in due isotopi stabili 12C e 13C . La loro presenza in percentuale è rispettivamente pari a 98,89% e 1,11% Il fatto è che il rapporto fra i due isotopi può variare per le reazioni biochimiche naturali e le analoghe reazioni di laboratorio: per le prime, a causa dei processi di attraversamento delle membrane, si ha un leggero vantaggio per l'isotopo più leggero, meno rallentato rispetto all'isotopo di massa maggiore. In altre parole, sebbene dal punto di vista della reattività chimica i due isotopi siano indistinguibili, il fatto che l'isotopo più leggero diffonda più rapidamente può favorire reazioni contenenti l'isotopo 12C.
Per comprendere gli aspetti pratici della legge di Graham, possiamo citare due esempi interessanti:
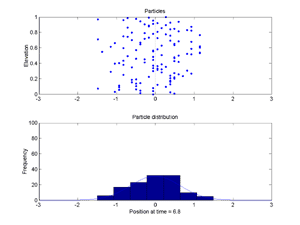 Il processo di diffusione con il quale un gas occupa tutto il volume a sua disposizione, comporta una ridistribuzione dell'energia cinetica media delle sue molecole. Questa ridistribuzione è mostrata nell'animazione qui proposta.
Nella parte superiore dell'animazione, 125 particelle sono seguite mentre si muovono casualmente a destra e a sinistra.
l'animazione è tratta da: http://www.ifh.uni-karlsruhe.de/ifh/studneu/envflu_I/Lecture_notes/lec2.htm |
| 2 | |||
Marcello Guidotti, copyright 2003, 2006, 2007, 2011
questa pagina può essere riprodotta su qualsiasi supporto o rivista purché sia citata la fonte e l'indirizzo di questo sito (ai sensi degli artt. 2575 e 2576 cc. Legislazione sul diritto d'autore). Le fotografie sono tratte da siti web e sono, o possono ritenersi, di pubblico dominio purché utilizzate senza fini di lucro. Le immagini di prodotti presenti nel sito hanno unicamente valenza esemplificativa oltre che, eventualmente, illustrare messaggi fuorvianti e non vi è alcun richiamo diretto o indiretto alla loro qualità e/o efficacia il cui controllo è affidato alle autorità regolamentatorie.