 fig. 1: a sinistra il chip Hurel; a destra la sua schematizzazione grafica |
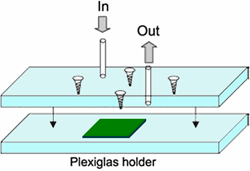 fig. 2: il chip all'interno della struttura di protezione che viene collegata ad una micropompa esterna |
Si definisce Test in Vitro una specifica categoria di Metodi Alternativi alla Sperimentazione Animale che impiega Sistemi Biologici semplificati (Colture Cellulari) o sofisticati (Organi e Tessuti Ricostruiti), Sistemi Artificiali Chimici o Fisici o Programmi Computerizzati
tratto dal Draft di - Understanding of Safety Evaluation of Finished Cosmetic Products (considering a Ban on Animal Testing) Commissione Europea - DG enterprise, Brussells 2001
Per ricavare le equazioni risolutive dei modelli bicompartimentali, e, più in generale, multicompartimentali, è necessaria la conoscenza delle costanti di trasferimento (le costanti cinetiche che regolano i flussi tra due compartimenti contigui), che però possono essere ottenute solo mediante sperimentazione animale, con il sacrificio degli stessi.
|
la direttiva CEE n. 609/86
La direttiva (CEE) n. 609/86 in materia di protezione degli animali utilizzati a fini sperimentali o ad altri fini scientifici", è la norma che si occupa della sperimentazione dal punto di vista degli animali stessi, mirando a proteggerli quando vengono utilizzati a tali fini scientifici: principio etico fondamentale nella sperimentazione animale è che gli animali da esperimento non devono essere sottoposti a maltrattamenti e sofferenze evitabili. In particolare, l'articolo 7.2 della Direttiva afferma che: "Si eviterà di eseguire un esperimento qualora per ottenere il risultato ricercato sia ragionevolmente e praticamente applicabile un altro metodo, scientificamente valido, che non implichi l'impiego di animali." Poiché nel termine "ragionevolmente e praticamente applicabile" potrebbero individuarsi ambiguità atte ad eludere la direttiva, nella sua stesura si è introdotto l'articolo 23.1, secondo il quale: "La Commissione e gli Stati membri dovrebbero incoraggiare la ricerca intesa a sviluppare e rendere più efficaci tecniche alternative atte a fornire lo stesso livello d'informazione degli esperimenti su animali ma che prevedano l'utilizzo di un minor numero di animali o comportino procedimenti meno dolorosi e prendono tutte le misure che ritengono opportune per favorire la ricerca in questo settore. La Commissione e gli Stati membri seguono l'evoluzione dei metodi sperimentali". |
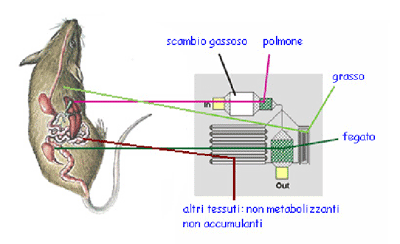
 fig. 1: a sinistra il chip Hurel; a destra la sua schematizzazione grafica |
 fig. 2: il chip all'interno della struttura di protezione che viene collegata ad una micropompa esterna |
Dal 2004, proseguendo le ricerche iniziate alla Cornell University (Ithaca, New York State) la società Hurel ha studiato un'alternativa in vitro compatibile con la risoluzione dei modelli PBPK (Phisiologically Based Pharmaco Kinetic). Questa alternativa è costituita da un chip ibrido in cui una parte della componentistica elettronica è costituita da celle (compartimenti) contenenti cellule animali.
Uno dei modelli CCA (Cell Culture Analog, Coltura Analogo Cellulare) realizzati dalla Hurel (fig. 1) comprende quattro compartimenti (polmone, fegato, altri tessuti e grasso). I compartimenti "polmone", "fegato" e "grasso" contengono cellule viventi, il compartimento "altri tessuti" (o tessuti rapidamente perfusi), invece, non contiene cellule ma simula la distribuzione del fluido nei tessuti non metabolizzanti e non accumulanti. Ogni compartimento contiene una coltura di cellule di mammifero specificamente selezionata per simulare-mimare i diversi sistemi "organo": tali compartimenti-organo, collegati da un mezzo di coltura circolante che scorrendo all'interno di canali microfluidici simula il sistema circolatorio, sono progettati su parametri quali il tempo di permanenza e il flusso di distribuzione ai vari compartimenti nel corrispondente modello PBPK.
Il fluido circolante (DMEM/F12 integrato con FBS), che costituisce un surrogato del sangue, è alimentato da una pompa peristaltica che garantisce un flusso di 0.76 μL/min ed è progettato in modo da mantenere la vitalità cellulare delle colture di mammifero nel dispositivo μCCA, per almeno 24 ore. La diversificazione del flusso destinato ai diversi compartimenti (il 9, 25, e 66 % dei fluidi entrano, rispettivamente, nei compartimenti grasso, fegato e altri tessuti) è ottenuta incidendo a profondità diverse i microcanali sulla base di silicio del chip.
Il sistema μCCA (fig. 2), è costituito da un chip al silicio di 2,54 cm2 (circa l'unghia di un dito) incorporato tra due elementi di plexiglas, ed è realizzato con la tecnologia della microfabbricazione, utilizzando la tecnica standard della litografia. Il vantaggio di questa tecnologia, risiede nell'utilizzare sostanzialmente gli stessi processi produttivi degli odierni chip, e dunque con costi paragonabili a questi ultimi.
 Poiché al CCA possono essere applicate cellule di mammifero derivanti da specie differenti, questo sistema, potenzialmente, permette di conoscere i profili tossicologici e farmacologici come estrapolazione da studi di specie incrociate. La precisione dei parametri del modello PBPK ottenuti dal CCA dipende molto dall'affinità del tessuto creato nei confronti del vivo. Inoltre, è importante che i compartimenti CCA ricreino un ambiente fisiologicamente realistico. Condizioni non fisiologiche nei parametri come la quantità di liquido nelle cellule e lo sforzo di taglio potrebbero portare a variazioni in più o meno rispetto al reale metabolismo ed alle funzionalità fisiologiche delle cellule.
Poiché al CCA possono essere applicate cellule di mammifero derivanti da specie differenti, questo sistema, potenzialmente, permette di conoscere i profili tossicologici e farmacologici come estrapolazione da studi di specie incrociate. La precisione dei parametri del modello PBPK ottenuti dal CCA dipende molto dall'affinità del tessuto creato nei confronti del vivo. Inoltre, è importante che i compartimenti CCA ricreino un ambiente fisiologicamente realistico. Condizioni non fisiologiche nei parametri come la quantità di liquido nelle cellule e lo sforzo di taglio potrebbero portare a variazioni in più o meno rispetto al reale metabolismo ed alle funzionalità fisiologiche delle cellule.
Sebbene si utilizzino linee cellulari per rappresentare un "compartimento organo", si deve riconoscere che ciò non è sufficiente per simulare gli organi veri e propri. Però, il sistema rappresenta un buon punto di partenza per una selezione più rigida dei candidati farmaci da condurre alla sperimentazione animale in quanto, oltre ad utilizzare tessuti appartenenti una volta a specie diverse e, in linea di principio, anche tessuti con specie incrociate, possono essere utilizzate anche tessuti appositamente progettati, in modo da poter riprodurre più strettamente le caratteristiche egli organi.
| 8 | ||||||||||||||
Marcello Guidotti, copyright 2008
questa pagina può essere riprodotta su qualsiasi supporto o rivista purché sia citata la fonte e l'indirizzo di questo sito (ai sensi degli artt. 2575 e 2576 cc. Legislazione sul diritto d'autore). Le fotografie sono tratte da siti web e sono, o possono ritenersi, di pubblico dominio purché utilizzate senza fini di lucro. Le immagini di prodotti presenti nel sito hanno unicamente valenza esemplificativa oltre che, eventualmente, illustrare messaggi fuorvianti e non vi è alcun richiamo diretto o indiretto alla loro qualità e/o efficacia il cui controllo è affidato alle autorità regolamentatorie.